今年の10月から導入されるインボイス制度。
税務職員の面接試験で尋ねられる可能性もあるので調べてみました。奥さんも個人事業主だしな。
ひとことでいうと、事業者は国が決めた適格請求書(インボイス)を発行しないと、消費税の免税対象にならなくなったってことらしい。
そもそものきっかけは、軽減税率の導入で、納税の不正やミスが問題になったため。
しかし、このインボイスの発行が鬼面倒くさいらしく、免税事業者(消費税の課税対象になる売上高が1000万円以下の事業主。消費税の納税を許されている)も、場合によってはインボイス発行事業者に登録しなければならず、SNSを中心に反対のシュプレヒコールが起きている。
仕入れ税額控除
クッキー屋がクッキーを売って設けた場合、売上高に消費税がかかり、その分を納税するのは当たり前だが、クッキーを作る材料にかかった消費税分が課税対象から差し引かれる。
たとえば、クッキーの売り上げが1万円だったら納税は1000円だが、材料費に税込7000円かかっていた場合は700円分は材料を買った店が納税しているはずなので、二重課税となり差し引かれる。よってクッキー屋の納税額は300円。
この仕入れ税額控除が、インボイスの請求書がないと受けられなくなるらしい。
つまり、今まで消費税を勘弁してもらっていた免税事業者はインボイスが出せないため、免税事業者へ仕事を依頼する取引先が減るかもしれないと危惧されているという。
ほかにも、消費税の上乗せ分、料金を値下げさせられるとか、課税事業者との競合に負ける(こっちに頼めば仕入れ税額控除が受けられるため)とかあるらしいが、取引先も免税事業者だった場合は、インボイスがなくても当面は控除ができるらしい。
免税事業者
メリット:消費税の納税義務がない
デメリット:消費税分値下げを要求される可能性。インボイス事業者との価格競争に負ける可能性。
課税事業者
メリット:仕入れ税額控除の対象になるため、安定した仕事の依頼。今後3年間は納税額に手心が加えられる(売上税額の2割で良い負担軽減措置)。
デメリット:インボイスの発行手続きが面倒(勘定奉行におまかせあれ)。消費税の納税があるので手取りが減る。
感想
素人目にはメリットがあまり見えてこず、政府は確実に税を取りたいんだなという(コンプライアンスを徹底させた公平な納税にはなるが)。
あと軽減税率を導入しなければ、この悲劇はなかった気がする(公明党のせい)。つーか、なんで新聞に軽減税率が適用されているのか解せぬ。まあ、もう誰も購読してないけど。
財務省の手先の宏池会系の岸田総理が槍玉に挙げられるが、実はインボイス制度の導入は平成27年の第三次安倍内閣においても槍玉に上がっていた。
ちなみに、当時の麻生財務大臣はこう答えている。
ヨーロッパも皆そうですけれども、これを導入したときに中小零細業者の事務負担が非常に増えることになりますので、その点を考えて免税点制度をやったり、あとは簡易課税制度を導入したりというのをいろいろヨーロッパではやっていることは承知しています。実際問題としていざこれをやっていくときには、そういった零細業者への配慮というものを考えて、いろいろ現実的な仕組みというものも考えなければいけないだろうなという感じはします。少し時間がかかるのだと思いますけれども、そういうことを考えていかなければいけないと思います。――金融庁での記者会見
麻生さんでさえ、こういっているのだから、もっとタイミングとかそういうのあったと思うよ。なぜ、新型コロナとウクライナ戦争で物価高の今なんだっていう。いや、インフレの今こそ!なのかな。とんでもねーな。
でも、今さら署名を集めて廃止になるのかな。もう来月だしな。ここまで来たら、インボイス制度そのものを廃止じゃなくて、中小零細企業は勘弁してもらえる温情的な制度をお願いしたほうが現実的だとは思う。ただし、岸田さんがそこまで甘い人間じゃないこともわかる。とんでもねーな。
R5年度東京都職員Ⅲ類採用試験について
2023-09-21 19:54:20 (2 years ago)
-
カテゴリタグ:
- 資格試験
全体的な感想
例年通りの内容が出題されたが、今年はかなり難しい。
特に、知識系の問題がかなり意地悪で、詐欺師の手口と言っても過言ではなかろう。
例年に比べて平均点はかなり下がると思われるが、もともと一次のクリアラインはかなり高い試験なので安心はできない(逆に二次面接にまで生き残れば期待値は高い)。
データ
全45題 時間は120分
試験問題持ち帰り可能。東京都の公式サイトにて閲覧も可能。
星の数は難易度。
☆:易しい。小中学生レベル。
☆☆:普通。高校生レベル。
☆☆☆:難しい。大学入試~大学生レベル。
※:判定不能。悪問や、出題ミスなど。
文章理解
内容は抽象的でかなり難しい(選択肢自体は選べる)。なんというか大学入試っぽい。
古典がないのが救いか。
1.内容把握☆☆
出典:太田直道『人間の時間』
深い衝撃と感動によって主観を運び去る「瞬間の美」について。
カントやベルクソン、キルケゴールなどの抽象的な哲学の引用が多く、こういう文章に慣れていないと、読解はかなり厳しい。
①畏敬美を感じることは「できなくなる」がまちがい。
②超越美(=瞬間美)は自然美や形象美ではないと述べている。
③正しい。
④「喧噪の中にあっても」がまちがい。※3段落目6行。
⑤「平均的で現実的な暮らしを送りながら」がおかしい。
こたえは③
2.内容把握☆☆
出典:日高敏隆『生きものの流儀』
ドイツの生物哲学者フォン・ユクスキュルの「環世界」についての内容。なかなか渋いところをついてくるなあ。確か、すっごい昔に大学入試で出題された気がする。
内容は易しくないが、選択肢そのものは選びやすい。
①動物が主体的に抽出し、自分の意味あるもの(エサや安全な休憩場所など)を構築したのが「環世界」。正しい。
②環境の変化については言及されていない。
③人間の環世界についても言及していない。
④動物にとっては客観的な環境よりも主観的な環世界が問題。
⑤環境という概念は明確になったのではなく逆に漠然としたものになった。
3.文章整序☆
出典:フランソワーズ・サガン『悲しみよ こんにちは』
元の文章は判らないが、おそらく小説。
シチュエーションをイメージすれば解けるはず。
私と父とアンヌ(おそらく姉妹)が朝食で食卓に座るシーン。
私は父とおそらく失恋したであろうアンヌに対して、気まずくなかなか顔を見ていないことに注意。
A:すでに父とアンヌは食卓で座っている。
D:私も座るが気まずくて2人の顔は見ていない。
E:沈黙に耐えられなくなり、2人の顔を見る私。
B:アンヌの顔はやつれていた。
F:2人は微笑んでいた。
C:幸福とは成功だと思っていたので、2人が微笑んでいるのは印象的だった。
B→F→Cが難しいが、他の選択肢がもっと不自然。
こたえは②
4.空欄補充☆
出典:吉田洋一『零の発見』
非常に易しい。
アラビア数字は「文字」なのでAは「筆算」だろう。
電卓の進歩で、狭められていく役割はB「計算数字」としての役割。
しかし、数字の表し方である記数法として、アラビア数字はやはり強いのでC「記録数字」D「困難」
これで、こたえが確定。こたえは⑤
英語
今年は世界中にファンが多い、あの超有名作品が登場。
毎年よくいろいろな原著を見つけてくるなあ。
すべての問題の英文が丸々1ページの長文なので読解力がいると思う。
5.内容把握
出典:ビアトリクス・ポター『グロースターの仕立て屋』
まさかの『ピーターラビット』
貧乏な仕立て屋が受けた大きな仕事をネズミたちが代わりに仕上げてくれたという内容。
こたえは③
6.内容把握
出典:ペーター・ヴォールレーベン『樹木たちの知られざる生活: 森林管理官が聴いた森の声』
森の間伐の仕方という専門的な内容。こたえは①
7.内容把握
出典:エリン・メイヤー『カルチャーマップ』
毎年出てくる自己啓発系。こたえは③
8.内容把握
出典:AAミルン『プー横丁にたった家』
理外の『くまのプーさん』
言わずと知れたナンセンス文学なので、何を言っているのかさっぱりわからない。
「スモール」とはウサギに付けられた名前なのか、あだ名なのか、それともミヤケンの「クラムボン」、ルイス・キャロルの「スナーク」みたいなものなのかさっぱりだ。
こたえは③
判断推理
相変わらず出題数が多いが、出題範囲と順番が例年ほとんど同じなので、傾向が分かりやすい。10~12は数的推理な気がするけど、まあいいや。
9.集合☆☆
ベン図を3つ作るいつものやつ。
1種類だけ、2種類、3種類すべての区画をすべて分けて、7区画計93人とする。
こたえは⑤
10.場合の数☆☆
10段の階段を、1段上る、2段上る、の2種類の上り方ができる場合、上り方は何通りあるかという問題。
n段目までの上り方をまとめる。
1段目までの上り方:1段の1通り
2段目までの上り方:1段→1段と2段の2通り
3段目までの上り方:1→1→1、1→2、2→1の3通り
4段目までの上り方:1→1→1→1、1→1→2、1→2→1、2→1→1、2→2の5通り
5段目までの上り方:8通り
・・・ここらへんで、1個前と2個前を足した数になっていることが判る(フィボナッチ数列)。
6段目:13通り
7段目:21通り
8段目:34通り
9段目:55通り
10段目:89通り
こたえ①
11.確率☆
突然とんでもなく易しい。
2つのサイコロの積が15未満は36通り中23通り。
割り切れないのでこたえは④
12.確率☆
4の倍数は下2桁が4の倍数なら4の倍数。
各桁で1~9しか使えないので、
12、16、24、28、
32、36、44、48、
53、56、64、68
72、76、84、88
92、96
の18通り。
百の位が9通りあるので、18×9
全ての組み合わせは9×9×9なので
18×9 / 9×9×9 = 2/9
こたえ④
13.論理☆
対偶を作るいつものやつ。
算〇→音〇 音×→算×
国〇→図〇 図×→国×
音〇→図× 図〇→音×
体〇→国× 国〇→体×
国〇→音×→算×より、こたえは②
数的処理
毎年けっこう難易度が高い。
14.利益算☆☆
二次方程式になってしまう嫌な問題。
商品1個当たりの値段をχ%上げると、売上個数は0.5χ%減るという関係の場合、売上金額が10.5%増えるときのχの値を求めるというもの。
%がわかりやすいように1個100円、そして0.5%がやっかいなので200個とする。
これで0.5%減る=1個減るとなる。
(100+χ)円 × (200-χ)個 = 20000円 × 1.105倍
20000+200χ-100χ-χ² = 22100
0=χ²-100χ+2100
0=(χ-30)(χ-70)
χ=30と70
こたえ③
15.通過算☆☆
まず、単位変換が必要(道のりがm、速さが時速であるため)。
時速90kmは秒速25m。
時速216kmは秒速68m。
通過算には珍しく、同一方向で競争をしているので・・・
Aの道のり = AとBの車両の長さ + Bの道のり
とならなければ、AはBを追い抜けない。
Aの車両の長さをχm、Bの速さをVBm/sとすると・・・
25m/s×93秒 = (χ+290)m + VBm/s×93秒
2325 = χ+290 + 93VB
χ=2035-93VB・・・①
今度は、BとCが逆方向にすれ違うので・・・
Bの道のり = BとCの車両の長さ - Cの道のり
Cの車両の長さはAの2倍なので2χmとすると・・・
VBm/s×8秒 = (2χ+290)m - 68m/s×8秒
2χ=190+8VB・・・②
①と②を連立方程式で解く。
VB=20m/s
χ=175mとなる。
こたえ③
16.角度☆
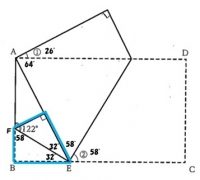
左下の折り返し部分から攻める。
△FBEは直角三角形。
よって∠FEB=32°
芋づる式に{180-(32×2)}÷2で
②が58°だと判明。
∠BEA=64°なので、錯角より∠EADも64°
①は90-64=26°
こたえ①
17.面積☆☆☆
ひらめきで解けず、純粋にムズイ。
ヘロンの公式か余弦定理を用いる。
①ヘロンの公式で解く場合
S=(10+17+21)/2=24
面積は24(24-10)(24-17)(24-21)の平方根。
24×14×7×3の平方根になるので
2×2×2×3 × 7×2 × 7 × 2 となり
4²×7²×3²の平方根となってくれる。
よって面積は4×3×7=84cm²
でこたえ①
➁余弦定理で解く場合
ヘロンでやっておけばと後悔したやつ。
とりあえず、底辺を21㎝として、辺10㎝の対角を∠Aとして
底辺21×高さ(sinA×17)÷2で解く。
∠Aを余弦定理で求める。
10²=17²+21²-2・17・21cosA
100=289+441-714cosA
714cosA=630
cosA=630/714=90/102=45/51=15/17
sin²A+cos²A=1より
χ²=64/17²
χ=8/17
sinA=8/17が分かったので、面積は
21× (8/17 ×17)÷2=84cm²
18.約数の個数☆
2000を素因数分解する。
2⁴×5³になるので
指数は4×3これにそれぞれ1を足して
5×4=20個
こたえ➁
資料解釈
例年ほとんど出題形式が同じ。とにかく問題の数が多い。
19.表☆☆
合計から%をかけて実質金額をいちいち出すのが面倒くさい。
①正しい。
②最大は絶対に令和3年※合計金額がまずデカい。
③茨城H30→R1は63336 東京都R1→R2は25686 よって3倍でない。
④令和3年が21%増。
⑤127485程となり、上回ってしまう。
こたえ①
20.棒グラフ☆
都営地下鉄の一日平均乗車数の推移。
絶対数なので易しい。
①17~20年までの浅草線の値をすべて足し4で割った数と、17年を比較する。
②18年:新宿/4路線 と 20年:新宿/4路線 を比較。
③19~21年の大江戸線富田線を比較。正しい。
④19~21年の 三田/浅草 を求め、すべてが0.9未満か検証。
⑤19年÷21年を各路線で求め、最も減少率が小さいのが大江戸線かを検証。ただし、棒グラフの高さ的に一目瞭然。
21.折れ線グラフ☆
地獄の対前年増加率。
①H28年の値を100として、30年までを足して3で割った値と、R1年の値を100として、R3年までを足して3で割った値を比較する。
計算例(肉用牛H28~30)
100 → 98?(約2%減) → 98×1.04(約4%増)
②H29年の鶏を100として、最後のR3年まで求める。辛い。後回し。
③これはベターなひっかけ。乳用牛の折れ線グラフは減少傾向に見えるが、R2年まではプラス域にいるので、すべて増加している(増加の度合いが下がっているだけで、毎年増えている)。
④これもひっかけ。R3年の肉用牛は前年のR2年で大きく減らした後なので、産出額が最大にはならない。
⑤R1年の鶏と豚を100として、R3年の値を出すと、鶏が113、豚102なので正しい。
22.割合つき棒グラフ☆☆
①どう考えても22年が最大。
②304803×51.7の値を100として、307367×43.9の値がいくつに駆るかを検証。
③19~21年のオーディオレコードと音楽ビデオの具体的な値をすべて出さなければならないので後回し。
④音楽ビデオ20~22年の具体的売り上げをすべて足して、3で割る。
20年:64619 21年:65696 22年:67620
65000に届かない、もしくは超えた値をすべて足して、マイナスにならなければ正しい。
-400、+700、+2600なので正しい。
⑤22年音楽配信は107%、音楽ビデオは94%なのでまちがい。
23.指数☆☆
20年のプロットがないが、20年の値を100とした指数であると、注釈があるのに注意。
①横浜の転入者(横軸)なので最も多いのは前年比プラスの21年。
②東京都特別区の転出者(縦軸)は大きく減らしている。
③東京都特別区も転入・転出ともに下がっている。
④転出者数(縦軸)は100→103→104なので、正しい。
⑤21年の転入者数は96%なのでまちがい。
判断推理
恒例の第二部。こっちは易しい。
24.平面構成☆
畳の敷き方。
40×30の外枠を20×30の上下2つに分けてはめていくと、3通りあるので、上下を踏まえて9通り。
また、真ん中を縦にまたぐパターンが左右2通りあるので、計11通り。
こたえ➁
25.折り紙☆
右下の△の模様を見れば一目瞭然。こたえ③
26.展開図☆
正八面体のベターな問題。こたえ③
27.軌跡☆
2つの円の回転を分けて考えないと絶対に混乱する。
円A、B、Cの円周は2πr、4πr、8πrとなる。
よって円Bは半回転して(2πr動いて)、円C上を移動。
円Aは1回転して(同じく2πr動いて)、円B上を移動。
こたえは⑤
28.軌跡☆
円周上の点の軌跡だと思って、サイクロイド曲線の積分に恐怖したが、円の軌跡の面積だった。
3a×6a=18a²の外枠から、まずa×4a=4a²の内枠を引く。
この時点で面積は14a²
そして、4か所の角を取っていくが、これはa×aの正方形の面積から直径aの円の面積を引いた値に等しい。
よって、14a²-{a²-(1πa²/4)}
こたえ④
教養問題
29.時事問題☆☆
情報通信技術について。
①AIはしょせんは計算機なので、人間のような知的活動はできない。
②IoTは、様々なものがネットにつながっているということ。
③サブスクとは、定額料金を払うコンテンツサービス。NHKやアマプラなど。
④eコマースの説明。正しい。
⑤VRではなくAR(拡張現実)の説明。
30.時事問題☆☆☆
世界人口について。
①19年に国連は2050年には人口は97億人になると予想。正しい。
②94年の国連人口開発会議はブカレストではなくカイロで開催。74年の世界人口会議がブカレスト。激ムズ。
③発展途上国は人口が爆発。
④先進国が人口が減少。
⑤21年の報告では、23億人が食糧不足。8億人が栄養不足。実は、食糧自体が足りないのではなく、分配がうまくいっていないことによる。激ムズ。
31.慣用句☆
A:「煮え湯を飲まされる」は、信頼をしていた人から裏切られること。
B:「琴線に触れる」は、感動すること。
C:「砂を噛むよう」は、味わいがないこと。
D:「手をこまねく」は、何もできず傍観していること。
E:「気が置けない」は、間違えやすいが、遠慮なく何でも言い合える間柄。※「気を置く
が気を使うという意味なため。
こたえは②
人文科学
総じてマニアックなうえに選択肢が悪質。まともに相手にしない方がいい。
32.日本史☆☆☆
大河ドラマ『鎌倉殿の13人』『北条時宗』『太平記』をしっかり視聴しても難しい問題。
①北条時政が後白河法皇に全国に守護・地頭を置くことを認めさせたのは1185年で、頼朝が征夷大将軍に任じられたのは後白河崩御後の1192年なので時期が違う。なんつーひっかけ。
②得宗専制政治の得宗はもともと「徳宗」で、北条義時がなくなった際に送られた号にちなむ。マニアック!そして義時は徳のある政治家だったのだろうか。
③北条時頼ではなく、3代執権北条泰時の記述。
④1回目の元寇(文永の役)を受けて、異国警固番役を新設ではなく“強化”した。ひっかけが詐欺師の手口。
⑤足利高氏は鎌倉ではなく京都の六波羅探題を攻めた。鎌倉の北条氏は高氏の息子をリーダーに、ライバルの新田義貞が滅ぼした。
33.日本史☆☆
室町時代の文化。
①東山文化ではなく北山文化。
②北山文化ではなく東山文化。
③『神皇正統記』は南朝についた北畠親房の歴史書なので、北朝の正統性は論じていない。
④能の真髄を述べた『風姿花伝』を残したのは世阿弥。正しい。
⑤雪舟は大和絵ではなく水墨画。
34.西洋史☆☆☆
共和制ローマと帝政ローマの出来事をしっかり区別しないと間違う。
①内乱の1世紀の説明は正しいが、この時はまだ共和制ローマ。
②オクタウィアヌスについての記述だが、プリンケプスとアウグストゥスの称号が逆。
③ポエニ戦争は共和制ローマの頃。
④コンスタンティヌス帝ではなくテオドシウス帝。
⑤“一時的に”という記述が気になるが、正しい。
35.西洋史☆☆
18世紀のアメリカ史。
①アメリカ植民地は、自分たちの代表がイギリス議会にいないのだから、議会の課税決定には承服できないとした。
②ボストン茶会事件のあとに、第1回大陸会議でイギリスと団結して戦うことを決めた。
③トマス=ジェファーソンの間違い。
④正しい。わりとアメリカ独立承認のパリ条約って出るな。
⑤パリ条約が1783、合衆国憲法が1787なので翌年ではない。また、州権主義ではなく、連邦主義が盛り込まれた。
36.地誌学☆☆
①フィジーは東南アジアではなくオセアニア州。
②日本同様、季節風は夏に湿潤、冬に乾燥なのでまちがい。
③東南アジアの棚田の説明。正しい。
④ベトナムのドイモイ政策は市場経済への移行。
⑤フィリピンはスペインやアメリカの影響でクリスチャンが多い。
37.自然地理学☆
日本の地形。
①日本の国土は約37万平方キロ。日本最南端は沖ノ鳥島。
②日本海溝は日本海にはない!太平洋側。
③日本アルプスは飛騨、木曽、赤石山脈で、中央アルプスは木曽山脈。
④最大の流域面積を持つ川は利根川。
⑤正しい。
社会科学
公務員試験に頻出の範囲ばかりが素直に出題された。
38.政治学☆
日本の選挙制度。
①正しい。
②参議院選挙の比例区は非拘束名簿方式。
③一票の格差は最高裁が違憲判決を出している。よく出るな、これ。
④秘密選挙(だれに投票したかはバレない)はもちろん禁止されていない。
⑤インターネット選挙各堂は解禁。これもよく出るな。
39.政治学☆☆
地方自治の記述。③と⑤で悩む。
①団体自治(中央政府から独立して地方公共団体が自治を行う)は廃止されていない。というか、住民自治と団体自治は兼ねられる。
②機関委任事務は廃止され、法定受託事務に。
③正しい。地方自治はアメリカ大統領制に近い。
④条例の制定・改廃請求(イニシアティブ)の必要署名数は有権者の1/50
⑤条例は法律の範囲内で制定されるが、情報公開に関しては地方が国に先んじている。山形の情報公開条例が1982年、情報公開法の施行は2001年。
40.経済学☆
市場経済について。易しい。
①カルテルとトラストの説明が逆。
②外部経済ではなく、外部不経済の説明。
③公共財の説明。正しい。
④均衡価格ではなく管理価格という。
⑤消費者庁ではなく、公正取引委員会。
41.経済学☆
国民所得と経済成長。易しい。
①ストックではなくフロー。
②国民総所得GNIはストック(国富)ではなくフロー。
③国内総生産-固定資本減耗で国内純生産。
④三面等価の原則の説明。正しい。
⑤名目経済成長率と実質経済成長率が逆。
自然科学
自然科学はすべて易しい。ここで満点を取って稼ぎたい。
42.物理学☆
力のモーメント。
左側=右側
20cm・χkg + 40cm・1kg = 30cm・4kg
χ=4kg
こたえ④
43.化学☆
中和滴定の計算。水酸化バリウムも硫酸もどちらも2価。
2価・0.1mol/L・200mL=2価・0.2mol/L・χmL
χ=100mL
こたえ②
44.生物学☆
ヒトの血液。
①有形成分で最も多いのは赤血球。
②血漿は91%が水分。
③正しい。
④白血球ではなく血小板の説明。
⑤血小板ではなく白血球の説明。
45.地学☆
①火山岩ではなく深成岩。
②火成岩ではなく造岩鉱物の説明だし、成分金属が逆。
③堆積岩の説明。正しい。
④ホルンフェルスは接触変成作用。
⑤大理石はもとは石灰岩が接触変成作用で結晶に。
例年通りの内容が出題されたが、今年はかなり難しい。
特に、知識系の問題がかなり意地悪で、詐欺師の手口と言っても過言ではなかろう。
例年に比べて平均点はかなり下がると思われるが、もともと一次のクリアラインはかなり高い試験なので安心はできない(逆に二次面接にまで生き残れば期待値は高い)。
データ
全45題 時間は120分
試験問題持ち帰り可能。東京都の公式サイトにて閲覧も可能。
星の数は難易度。
☆:易しい。小中学生レベル。
☆☆:普通。高校生レベル。
☆☆☆:難しい。大学入試~大学生レベル。
※:判定不能。悪問や、出題ミスなど。
文章理解
内容は抽象的でかなり難しい(選択肢自体は選べる)。なんというか大学入試っぽい。
古典がないのが救いか。
1.内容把握☆☆
出典:太田直道『人間の時間』
深い衝撃と感動によって主観を運び去る「瞬間の美」について。
カントやベルクソン、キルケゴールなどの抽象的な哲学の引用が多く、こういう文章に慣れていないと、読解はかなり厳しい。
①畏敬美を感じることは「できなくなる」がまちがい。
②超越美(=瞬間美)は自然美や形象美ではないと述べている。
③正しい。
④「喧噪の中にあっても」がまちがい。※3段落目6行。
⑤「平均的で現実的な暮らしを送りながら」がおかしい。
こたえは③
2.内容把握☆☆
出典:日高敏隆『生きものの流儀』
ドイツの生物哲学者フォン・ユクスキュルの「環世界」についての内容。なかなか渋いところをついてくるなあ。確か、すっごい昔に大学入試で出題された気がする。
内容は易しくないが、選択肢そのものは選びやすい。
①動物が主体的に抽出し、自分の意味あるもの(エサや安全な休憩場所など)を構築したのが「環世界」。正しい。
②環境の変化については言及されていない。
③人間の環世界についても言及していない。
④動物にとっては客観的な環境よりも主観的な環世界が問題。
⑤環境という概念は明確になったのではなく逆に漠然としたものになった。
3.文章整序☆
出典:フランソワーズ・サガン『悲しみよ こんにちは』
元の文章は判らないが、おそらく小説。
シチュエーションをイメージすれば解けるはず。
私と父とアンヌ(おそらく姉妹)が朝食で食卓に座るシーン。
私は父とおそらく失恋したであろうアンヌに対して、気まずくなかなか顔を見ていないことに注意。
A:すでに父とアンヌは食卓で座っている。
D:私も座るが気まずくて2人の顔は見ていない。
E:沈黙に耐えられなくなり、2人の顔を見る私。
B:アンヌの顔はやつれていた。
F:2人は微笑んでいた。
C:幸福とは成功だと思っていたので、2人が微笑んでいるのは印象的だった。
B→F→Cが難しいが、他の選択肢がもっと不自然。
こたえは②
4.空欄補充☆
出典:吉田洋一『零の発見』
非常に易しい。
アラビア数字は「文字」なのでAは「筆算」だろう。
電卓の進歩で、狭められていく役割はB「計算数字」としての役割。
しかし、数字の表し方である記数法として、アラビア数字はやはり強いのでC「記録数字」D「困難」
これで、こたえが確定。こたえは⑤
英語
今年は世界中にファンが多い、あの超有名作品が登場。
毎年よくいろいろな原著を見つけてくるなあ。
すべての問題の英文が丸々1ページの長文なので読解力がいると思う。
5.内容把握
出典:ビアトリクス・ポター『グロースターの仕立て屋』
まさかの『ピーターラビット』
貧乏な仕立て屋が受けた大きな仕事をネズミたちが代わりに仕上げてくれたという内容。
こたえは③
6.内容把握
出典:ペーター・ヴォールレーベン『樹木たちの知られざる生活: 森林管理官が聴いた森の声』
森の間伐の仕方という専門的な内容。こたえは①
7.内容把握
出典:エリン・メイヤー『カルチャーマップ』
毎年出てくる自己啓発系。こたえは③
8.内容把握
出典:AAミルン『プー横丁にたった家』
理外の『くまのプーさん』
言わずと知れたナンセンス文学なので、何を言っているのかさっぱりわからない。
「スモール」とはウサギに付けられた名前なのか、あだ名なのか、それともミヤケンの「クラムボン」、ルイス・キャロルの「スナーク」みたいなものなのかさっぱりだ。
こたえは③
判断推理
相変わらず出題数が多いが、出題範囲と順番が例年ほとんど同じなので、傾向が分かりやすい。10~12は数的推理な気がするけど、まあいいや。
9.集合☆☆
ベン図を3つ作るいつものやつ。
1種類だけ、2種類、3種類すべての区画をすべて分けて、7区画計93人とする。
こたえは⑤
10.場合の数☆☆
10段の階段を、1段上る、2段上る、の2種類の上り方ができる場合、上り方は何通りあるかという問題。
n段目までの上り方をまとめる。
1段目までの上り方:1段の1通り
2段目までの上り方:1段→1段と2段の2通り
3段目までの上り方:1→1→1、1→2、2→1の3通り
4段目までの上り方:1→1→1→1、1→1→2、1→2→1、2→1→1、2→2の5通り
5段目までの上り方:8通り
・・・ここらへんで、1個前と2個前を足した数になっていることが判る(フィボナッチ数列)。
6段目:13通り
7段目:21通り
8段目:34通り
9段目:55通り
10段目:89通り
こたえ①
11.確率☆
突然とんでもなく易しい。
2つのサイコロの積が15未満は36通り中23通り。
割り切れないのでこたえは④
12.確率☆
4の倍数は下2桁が4の倍数なら4の倍数。
各桁で1~9しか使えないので、
12、16、24、28、
32、36、44、48、
53、56、64、68
72、76、84、88
92、96
の18通り。
百の位が9通りあるので、18×9
全ての組み合わせは9×9×9なので
18×9 / 9×9×9 = 2/9
こたえ④
13.論理☆
対偶を作るいつものやつ。
算〇→音〇 音×→算×
国〇→図〇 図×→国×
音〇→図× 図〇→音×
体〇→国× 国〇→体×
国〇→音×→算×より、こたえは②
数的処理
毎年けっこう難易度が高い。
14.利益算☆☆
二次方程式になってしまう嫌な問題。
商品1個当たりの値段をχ%上げると、売上個数は0.5χ%減るという関係の場合、売上金額が10.5%増えるときのχの値を求めるというもの。
%がわかりやすいように1個100円、そして0.5%がやっかいなので200個とする。
これで0.5%減る=1個減るとなる。
(100+χ)円 × (200-χ)個 = 20000円 × 1.105倍
20000+200χ-100χ-χ² = 22100
0=χ²-100χ+2100
0=(χ-30)(χ-70)
χ=30と70
こたえ③
15.通過算☆☆
まず、単位変換が必要(道のりがm、速さが時速であるため)。
時速90kmは秒速25m。
時速216kmは秒速68m。
通過算には珍しく、同一方向で競争をしているので・・・
Aの道のり = AとBの車両の長さ + Bの道のり
とならなければ、AはBを追い抜けない。
Aの車両の長さをχm、Bの速さをVBm/sとすると・・・
25m/s×93秒 = (χ+290)m + VBm/s×93秒
2325 = χ+290 + 93VB
χ=2035-93VB・・・①
今度は、BとCが逆方向にすれ違うので・・・
Bの道のり = BとCの車両の長さ - Cの道のり
Cの車両の長さはAの2倍なので2χmとすると・・・
VBm/s×8秒 = (2χ+290)m - 68m/s×8秒
2χ=190+8VB・・・②
①と②を連立方程式で解く。
VB=20m/s
χ=175mとなる。
こたえ③
16.角度☆

左下の折り返し部分から攻める。
△FBEは直角三角形。
よって∠FEB=32°
芋づる式に{180-(32×2)}÷2で
②が58°だと判明。
∠BEA=64°なので、錯角より∠EADも64°
①は90-64=26°
こたえ①
17.面積☆☆☆
ひらめきで解けず、純粋にムズイ。
ヘロンの公式か余弦定理を用いる。
①ヘロンの公式で解く場合
S=(10+17+21)/2=24
面積は24(24-10)(24-17)(24-21)の平方根。
24×14×7×3の平方根になるので
2×2×2×3 × 7×2 × 7 × 2 となり
4²×7²×3²の平方根となってくれる。
よって面積は4×3×7=84cm²
でこたえ①
➁余弦定理で解く場合
ヘロンでやっておけばと後悔したやつ。
とりあえず、底辺を21㎝として、辺10㎝の対角を∠Aとして
底辺21×高さ(sinA×17)÷2で解く。
∠Aを余弦定理で求める。
10²=17²+21²-2・17・21cosA
100=289+441-714cosA
714cosA=630
cosA=630/714=90/102=45/51=15/17
sin²A+cos²A=1より
χ²=64/17²
χ=8/17
sinA=8/17が分かったので、面積は
21× (8/17 ×17)÷2=84cm²
18.約数の個数☆
2000を素因数分解する。
2⁴×5³になるので
指数は4×3これにそれぞれ1を足して
5×4=20個
こたえ➁
資料解釈
例年ほとんど出題形式が同じ。とにかく問題の数が多い。
19.表☆☆
合計から%をかけて実質金額をいちいち出すのが面倒くさい。
①正しい。
②最大は絶対に令和3年※合計金額がまずデカい。
③茨城H30→R1は63336 東京都R1→R2は25686 よって3倍でない。
④令和3年が21%増。
⑤127485程となり、上回ってしまう。
こたえ①
20.棒グラフ☆
都営地下鉄の一日平均乗車数の推移。
絶対数なので易しい。
①17~20年までの浅草線の値をすべて足し4で割った数と、17年を比較する。
②18年:新宿/4路線 と 20年:新宿/4路線 を比較。
③19~21年の大江戸線富田線を比較。正しい。
④19~21年の 三田/浅草 を求め、すべてが0.9未満か検証。
⑤19年÷21年を各路線で求め、最も減少率が小さいのが大江戸線かを検証。ただし、棒グラフの高さ的に一目瞭然。
21.折れ線グラフ☆
地獄の対前年増加率。
①H28年の値を100として、30年までを足して3で割った値と、R1年の値を100として、R3年までを足して3で割った値を比較する。
計算例(肉用牛H28~30)
100 → 98?(約2%減) → 98×1.04(約4%増)
②H29年の鶏を100として、最後のR3年まで求める。辛い。後回し。
③これはベターなひっかけ。乳用牛の折れ線グラフは減少傾向に見えるが、R2年まではプラス域にいるので、すべて増加している(増加の度合いが下がっているだけで、毎年増えている)。
④これもひっかけ。R3年の肉用牛は前年のR2年で大きく減らした後なので、産出額が最大にはならない。
⑤R1年の鶏と豚を100として、R3年の値を出すと、鶏が113、豚102なので正しい。
22.割合つき棒グラフ☆☆
①どう考えても22年が最大。
②304803×51.7の値を100として、307367×43.9の値がいくつに駆るかを検証。
③19~21年のオーディオレコードと音楽ビデオの具体的な値をすべて出さなければならないので後回し。
④音楽ビデオ20~22年の具体的売り上げをすべて足して、3で割る。
20年:64619 21年:65696 22年:67620
65000に届かない、もしくは超えた値をすべて足して、マイナスにならなければ正しい。
-400、+700、+2600なので正しい。
⑤22年音楽配信は107%、音楽ビデオは94%なのでまちがい。
23.指数☆☆
20年のプロットがないが、20年の値を100とした指数であると、注釈があるのに注意。
①横浜の転入者(横軸)なので最も多いのは前年比プラスの21年。
②東京都特別区の転出者(縦軸)は大きく減らしている。
③東京都特別区も転入・転出ともに下がっている。
④転出者数(縦軸)は100→103→104なので、正しい。
⑤21年の転入者数は96%なのでまちがい。
判断推理
恒例の第二部。こっちは易しい。
24.平面構成☆
畳の敷き方。
40×30の外枠を20×30の上下2つに分けてはめていくと、3通りあるので、上下を踏まえて9通り。
また、真ん中を縦にまたぐパターンが左右2通りあるので、計11通り。
こたえ➁
25.折り紙☆
右下の△の模様を見れば一目瞭然。こたえ③
26.展開図☆
正八面体のベターな問題。こたえ③
27.軌跡☆
2つの円の回転を分けて考えないと絶対に混乱する。
円A、B、Cの円周は2πr、4πr、8πrとなる。
よって円Bは半回転して(2πr動いて)、円C上を移動。
円Aは1回転して(同じく2πr動いて)、円B上を移動。
こたえは⑤
28.軌跡☆
円周上の点の軌跡だと思って、サイクロイド曲線の積分に恐怖したが、円の軌跡の面積だった。
3a×6a=18a²の外枠から、まずa×4a=4a²の内枠を引く。
この時点で面積は14a²
そして、4か所の角を取っていくが、これはa×aの正方形の面積から直径aの円の面積を引いた値に等しい。
よって、14a²-{a²-(1πa²/4)}
こたえ④
教養問題
29.時事問題☆☆
情報通信技術について。
①AIはしょせんは計算機なので、人間のような知的活動はできない。
②IoTは、様々なものがネットにつながっているということ。
③サブスクとは、定額料金を払うコンテンツサービス。NHKやアマプラなど。
④eコマースの説明。正しい。
⑤VRではなくAR(拡張現実)の説明。
30.時事問題☆☆☆
世界人口について。
①19年に国連は2050年には人口は97億人になると予想。正しい。
②94年の国連人口開発会議はブカレストではなくカイロで開催。74年の世界人口会議がブカレスト。激ムズ。
③発展途上国は人口が爆発。
④先進国が人口が減少。
⑤21年の報告では、23億人が食糧不足。8億人が栄養不足。実は、食糧自体が足りないのではなく、分配がうまくいっていないことによる。激ムズ。
31.慣用句☆
A:「煮え湯を飲まされる」は、信頼をしていた人から裏切られること。
B:「琴線に触れる」は、感動すること。
C:「砂を噛むよう」は、味わいがないこと。
D:「手をこまねく」は、何もできず傍観していること。
E:「気が置けない」は、間違えやすいが、遠慮なく何でも言い合える間柄。※「気を置く
が気を使うという意味なため。
こたえは②
人文科学
総じてマニアックなうえに選択肢が悪質。まともに相手にしない方がいい。
32.日本史☆☆☆
大河ドラマ『鎌倉殿の13人』『北条時宗』『太平記』をしっかり視聴しても難しい問題。
①北条時政が後白河法皇に全国に守護・地頭を置くことを認めさせたのは1185年で、頼朝が征夷大将軍に任じられたのは後白河崩御後の1192年なので時期が違う。なんつーひっかけ。
②得宗専制政治の得宗はもともと「徳宗」で、北条義時がなくなった際に送られた号にちなむ。マニアック!そして義時は徳のある政治家だったのだろうか。
③北条時頼ではなく、3代執権北条泰時の記述。
④1回目の元寇(文永の役)を受けて、異国警固番役を新設ではなく“強化”した。ひっかけが詐欺師の手口。
⑤足利高氏は鎌倉ではなく京都の六波羅探題を攻めた。鎌倉の北条氏は高氏の息子をリーダーに、ライバルの新田義貞が滅ぼした。
33.日本史☆☆
室町時代の文化。
①東山文化ではなく北山文化。
②北山文化ではなく東山文化。
③『神皇正統記』は南朝についた北畠親房の歴史書なので、北朝の正統性は論じていない。
④能の真髄を述べた『風姿花伝』を残したのは世阿弥。正しい。
⑤雪舟は大和絵ではなく水墨画。
34.西洋史☆☆☆
共和制ローマと帝政ローマの出来事をしっかり区別しないと間違う。
①内乱の1世紀の説明は正しいが、この時はまだ共和制ローマ。
②オクタウィアヌスについての記述だが、プリンケプスとアウグストゥスの称号が逆。
③ポエニ戦争は共和制ローマの頃。
④コンスタンティヌス帝ではなくテオドシウス帝。
⑤“一時的に”という記述が気になるが、正しい。
35.西洋史☆☆
18世紀のアメリカ史。
①アメリカ植民地は、自分たちの代表がイギリス議会にいないのだから、議会の課税決定には承服できないとした。
②ボストン茶会事件のあとに、第1回大陸会議でイギリスと団結して戦うことを決めた。
③トマス=ジェファーソンの間違い。
④正しい。わりとアメリカ独立承認のパリ条約って出るな。
⑤パリ条約が1783、合衆国憲法が1787なので翌年ではない。また、州権主義ではなく、連邦主義が盛り込まれた。
36.地誌学☆☆
①フィジーは東南アジアではなくオセアニア州。
②日本同様、季節風は夏に湿潤、冬に乾燥なのでまちがい。
③東南アジアの棚田の説明。正しい。
④ベトナムのドイモイ政策は市場経済への移行。
⑤フィリピンはスペインやアメリカの影響でクリスチャンが多い。
37.自然地理学☆
日本の地形。
①日本の国土は約37万平方キロ。日本最南端は沖ノ鳥島。
②日本海溝は日本海にはない!太平洋側。
③日本アルプスは飛騨、木曽、赤石山脈で、中央アルプスは木曽山脈。
④最大の流域面積を持つ川は利根川。
⑤正しい。
社会科学
公務員試験に頻出の範囲ばかりが素直に出題された。
38.政治学☆
日本の選挙制度。
①正しい。
②参議院選挙の比例区は非拘束名簿方式。
③一票の格差は最高裁が違憲判決を出している。よく出るな、これ。
④秘密選挙(だれに投票したかはバレない)はもちろん禁止されていない。
⑤インターネット選挙各堂は解禁。これもよく出るな。
39.政治学☆☆
地方自治の記述。③と⑤で悩む。
①団体自治(中央政府から独立して地方公共団体が自治を行う)は廃止されていない。というか、住民自治と団体自治は兼ねられる。
②機関委任事務は廃止され、法定受託事務に。
③正しい。地方自治はアメリカ大統領制に近い。
④条例の制定・改廃請求(イニシアティブ)の必要署名数は有権者の1/50
⑤条例は法律の範囲内で制定されるが、情報公開に関しては地方が国に先んじている。山形の情報公開条例が1982年、情報公開法の施行は2001年。
40.経済学☆
市場経済について。易しい。
①カルテルとトラストの説明が逆。
②外部経済ではなく、外部不経済の説明。
③公共財の説明。正しい。
④均衡価格ではなく管理価格という。
⑤消費者庁ではなく、公正取引委員会。
41.経済学☆
国民所得と経済成長。易しい。
①ストックではなくフロー。
②国民総所得GNIはストック(国富)ではなくフロー。
③国内総生産-固定資本減耗で国内純生産。
④三面等価の原則の説明。正しい。
⑤名目経済成長率と実質経済成長率が逆。
自然科学
自然科学はすべて易しい。ここで満点を取って稼ぎたい。
42.物理学☆
力のモーメント。
左側=右側
20cm・χkg + 40cm・1kg = 30cm・4kg
χ=4kg
こたえ④
43.化学☆
中和滴定の計算。水酸化バリウムも硫酸もどちらも2価。
2価・0.1mol/L・200mL=2価・0.2mol/L・χmL
χ=100mL
こたえ②
44.生物学☆
ヒトの血液。
①有形成分で最も多いのは赤血球。
②血漿は91%が水分。
③正しい。
④白血球ではなく血小板の説明。
⑤血小板ではなく白血球の説明。
45.地学☆
①火山岩ではなく深成岩。
②火成岩ではなく造岩鉱物の説明だし、成分金属が逆。
③堆積岩の説明。正しい。
④ホルンフェルスは接触変成作用。
⑤大理石はもとは石灰岩が接触変成作用で結晶に。
にゃんちゃん風邪をひく
2023-09-17 19:28:12 (2 years ago)
-
カテゴリタグ:
- 育児
近年「ハイハイ」を覚え、行動速度が異常に上がったにゃんちゃん。ますます目が離せません。しかも、そこらじゅうのものをひっくり返す傍若無人ぶりで、ひっくり返す前にものを取り上げると泣く始末。恐るべきモンスターに成長しました。
つーか、「手をパチパチ」「バイバイ」など、アクションを一つずつ覚えていく様が、アニマそのものである。「見て見て~」ってか。

そして、ついに人生初の風邪をひきました。※体温38.3℃を記録。あずさの兄貴の回復を祈るばかりである。
つーか、「手をパチパチ」「バイバイ」など、アクションを一つずつ覚えていく様が、アニマそのものである。「見て見て~」ってか。

そして、ついに人生初の風邪をひきました。※体温38.3℃を記録。あずさの兄貴の回復を祈るばかりである。
R5年度東京消防庁採用試験について
2023-09-14 21:28:36 (2 years ago)
-
カテゴリタグ:
- 資格試験
全体的な感想
昨年度から国家一般と日程をかぶせてきたので、どちらかしか受験できなくなった。
難易度は易しすぎず、難しすぎずといった感じ。
データ
全45題 時間は120分
試験問題持ち帰り可能。※解答は公式サイトにアップロード(解説はなし)
星の数は難易度。
☆:易しい。小中学生レベル。
☆☆:普通。高校生レベル。
☆☆☆:難しい。大学入試~大学生レベル。
文章理解
非常に易しい。後半の知識問題がやや難しいので、ここで点数を稼ぎたい。
今年のチョイスはまあまあの面白さだった。
1.内容把握☆
メディアという言葉は様々な意味で使われているよというだけの内容。
こたえは③
2.内容把握☆
美術史についての文章。洞窟壁画などの為政者が権威を示すための美術を不動産美術、15世紀以降のポータブルな流通可能な作品を動産美術と定義している。
選択肢が簡単すぎる。こたえは⑤
3.内容把握☆☆
多数決というシステムに従順で、受動的に選挙で投票している人は、主体的な主権者といえないのではないかといった内容。
本文に合致する選択肢は他にもあるが、要旨として最も妥当なのは⑤
4.空欄補充☆
ヒトは基本的に理性ではなく情動によって行動しているという内容。
こたえは②
5.文章整序☆
生物の進化について。
ゴリラについて書かれている箇所のD→Cを持っているのは①か③か⑤
また、Eの「彼」とはゴリラのシルバーバックのことなので、D→C→Eで確定。
これで①か③
また、Aの「だから」はBの「すべての生命は同じ祖先でつながっている」を受けているので、こたえは①
英語
文章は短く、たいへん易しい。わたしでもできる。
6.英文の内容把握☆
魚にまぶたはないが、常に起きているわけではなく、人間のように寝ているよという内容。
①魚も寝る。
②魚は目を閉じられない。
③流れの静かな穏やかな場所で休む。
④正しい。
⑤だから魚は目を閉じられないって!
7.英文の空欄補充☆
たった3行の会話文。
A:マリリン、(わたしは)マサコです。
B:はい、マサコ!お会いできてうれしいわ。
C:すいませんが、あなたの名前を聞き取れませんでした。
こたえは③
8.英語☆
9月は英語でセプテンバー。
こたえは⑤
判断推理
スタンダードな難易度。
9.論理☆
対偶を作ればいいだけ。
ア:数〇→理〇 理×→数×
イ:社〇→理× 理〇→社×
ウ:数×→英× 英〇→数〇
エ:国〇→英〇 英×→国×
つなげてみると
国〇→英〇→数〇→理〇→社×
こたえは③
10.対応☆
Aの選んだ球技がすぐに確定する。
AとBが選んだのがラグビーか、バスケかで場合分け。
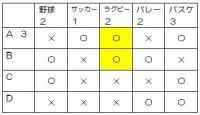
こちらの表はOK!
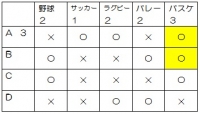
BとCが野球とバスケをともに選んでいるため、こっちはダメ。
こたえ②Bはラグビーを選んだ。
11.順序☆
仕事が遅い人は時間が大きい。
A:仕事最も遅い=時間大きい
E:仕事最も早い=時間小さい
A-E=20
A-C=11
B-E=13
C=28※5人の平均
28×5=140が全ての時間。
A=39
B=32
C=28
E=19
計118
140-118=22=D!
こたえ③CとDの差6はDとEの差3の2倍。
12.数量☆
5つの箱A~Eにはそれぞれ1,2,3,4,5枚のコインが入っている。
A>B ※A≠1
E>C ※E≠1
A=D+E ※Aは3以上
A=3とすると、D=1、E=2
ただし、A>Bなので無理。
A=4とすると、D=1、E=3、B=2、E=5
A=5とすると、D=2、E=3、B=4、C=1※E>Cのため
E=2、D=3、B=4、C=1
E=2、D=3、C=1、B=4
D=1、E=4、B=3、C=2
D=1、E=4、B=2、C=3
よって、可能なパターンは6通り。
こたえ②
13.平面構成☆
直角三角形の個数。
小×12
中×12
横長×6
半分×4
特大×2
合計④36個
14.平面構成☆
平面パズル。ほとんど同じ問題が問題集にある。
こたえ③
数的推理
約数・倍数、流水算、幾何学、場合の数など、代表的な問題をバランスよく出題。
15.約数・倍数☆
AとBは5:7で280の公約数。
5χ×7χ=280
35χ=280
χ=8
よってA=40、B=56
こたえ④
16.流水算☆
上り(減速)も下り(加速)も川の道のりは変わらない。
船の速さをχ、川の速さをyとする。
下りの道のり=上りの道のり
20分×(χ+y)=30分×(χ-y)
20χ+20y=30χ-30y
-10χ=-50y
χ=5y
つまり、船の速度は川の速度の5倍
下りの速度は、川の速度の6倍なので、川の流れだけで下ると、速度は1/6
よって、時間が6倍となる。
こたえ③120分
17.平面図形☆
たのしい数字合わせ。
P:12cm² 3×4
Q:36cm² 9×4
R:24cm² 3×8
なので
S:9×8
よってすべての辺を足すと、9+9+8+8=34cm
こたえ③
18.場合の数☆☆
わりとめんどうくさい。
1円と50円と100円が2枚ずつあるので、重複をはじけば50円刻みで考えると判りやすい。
1円 2円
50円 51円 52円
100円 101円 102円
150円 151円 152円
200円 201円 202円
250円 251円 252円
300円 301円 302円
こたえ③20通り
資料解釈
4問も出るのを忘れてた。が、特別区の100倍易しい。こういうのでいいんだよ。
19.表☆
これは易しい。
①18年の全項目を足せばよい。50%は超えないのはすぐにわかる。
②16年→20年なので、20年÷16年で計算
コーヒー豆:1.1倍
カカオ豆:1.28倍
茶:1.17倍
よって正しい。
③16年のみ。
④どう考えても3000千トンくらいしか多くない。
⑤指数は106なのでダメ。
20.表☆
①世界総計の30%を出せばいいから、0.3をかけると18年がダメ。
②10000千台を超える端数を足していくと、下回らない。
③5646×0.6=3387なので、60%未満。正しい。
④いけそうだが、21年がぎりぎりダメ。
⑤対前年減少“数”なので、日本ではなく中国。
21.グラフ☆
東京消防庁らしい火災の統計グラフ。
①グラフの高さを100で割って4倍する。すべて下回るので正しい。
②4053×0.8=3242なのでダメ。
③これも減少“数”なので、車両火災-119、林野火災-152なのでダメ。
④絶対違う。
⑤グラフの長さ的に16年が違うことは瞭然。
22.表&グラフ☆
①18年が怪しい(他は絶対違う)。1138305×0.63=717132なのでダメ。
②16年のアメリカは258729なので、その1.15倍は297538。ダメ。
③怪しい年(16年、17年、20年)だけを計算。
16年は124711、17年は85469、20年は99791。正しい。
④19年の日本99287の6倍は595725なのでダメ。ロシアは540800。
⑤17年アメリカ461090の50%は230545なのでダメ。18年アメリカは265225。
社会科学
スタンダードな難易度。
23.政治☆☆
基本的人権についてだが、ちょっとへんてこな問題。
ただし、不正解の選択肢が判りやすいので選びやすい。
①日本国憲法に法律の留保はない。
②公務員試験で初めて見た、栄典制度の説明。紫綬褒章など。正しい。
③投票の選択に私的な責任を問われるわけがない。
④憲法26条は「その能力に応じて」等しく教育を受ける権利を有する。
⑤団体行動権ももちろん保障される。
24.政治☆
憲法改正の発議は内閣ではなく国会。(憲法96条1項)
こたえ④
25.経済☆☆
①公共財は非競合性や非排除性を「持つ」。
②財政投融資は国債の一種である財投債で資金を調達する。
③ビルトインスタビライザーの説明。正しい。
④納入者と負担者が逆。
⑤水平的公平ではなく垂直的公平。
26.社会☆
日本の環境問題。
①汚染者負担の原則の説明。正しい。
②環境アセスメント法(97年公布)があるのでまちがい。
③3Rに特に優先順位はない。
④四台公害訴訟で原告側は勝訴。関係法令が見直され、賠償金も出た(しかし低かった)。
⑤環境基本法は93年に公布されたので、11年の東日本震災を受けて出来てはいない。
27.社会☆
育児休暇制度について。
A:子どもが原則1歳まで。
B:正しい。
C:正しい。
D:育休手当は会社ではなくハローワークから支給される。
人文科学
歴史の問題は経緯を時系列に並べる問題が多く、うろ覚えだとかなり厳しい。
28.西洋史☆☆
ロシア革命の流れの順番合わせ。
第一次世界大戦中に第二革命が成功し、ドイツと単独講和をして、戦後にソ連を成立させている。
C:サラエボ事件(1914)
B:第二ロシア革命(1917)
E:ブレスト=リトフスク条約(1918)
A:ソ連成立(1922)
D:スターリンが五か年計画スタート(1928)
こたえは④
29.西洋史☆
世界恐慌についての正誤問題。
ア:アメリカのニューディール政策の説明。正しい。
イ:マクドナルド内閣はフランスではなくイギリスの労働党政権。
ウ:ソ連の五か年計画は世界恐慌の影響を受けなかった。
エ:ヒトラーの公共事業の説明。正しい。
こたえは②
30.日本史☆
明治時代後半の流れの順番合わせ。
C:日清戦争(1894)
B:三国干渉(1895)※日清戦争で得た遼東半島を手放すことに。
E:日英同盟(1902)南下政策をするロシアを警戒。
A:日露戦争(1904)
D:韓国併合(1910)
こたえは③
31.日本史☆☆※
太平洋戦争についての記述。選択肢②が史観によっては正しい気もしないでもない。
この時代を出題するのはどうかと思う。
①ミッドウェー海戦に日本は敗北している。
②大東亜共栄圏はアジアエリアの白人植民地の開放が立て前。微妙。
③女子も勤労動員にかけられた。
④45年3月東京大空襲→4月沖縄戦→8月原子爆弾。正しい。
⑤ポツダム宣言を直ちに受諾していれば原爆は落とされなかった。
32.地理☆☆
エネルギーや鉱物について。
①西アジア(アラブ)の産油国はOPECではなくOAPEC。他は正しい。
②天然ガスは石油に比べて二酸化炭素排出量が少ないが、メタンガスの形で輸送中に漏れたりもするため、近年の発表では温暖化抑制効果は思ったよりも低いと言われている。
③世界に占める原子力発電の割合は3割弱。
④正しい。
⑤レアメタルは高価な金属ではなく、希少な金属のこと。プラチナやリチウム、コバルトなど。
33.地理☆
中国について。
ア:経済特区の記述。正しい。
イ:ウイグル族に対するジェノサイドの記述。正しい。
ウ:一人っ子政策の効果は抜群で、日本以上の少子高齢化になるとも言われている。
こたえは①
34.国語☆
漢字の書き。
①「異常」気象
②校庭を「開放」
③留学生と「交歓」正しい。
④「暗証」番号
⑤値段の「見当」
35.国語☆☆
四字熟語の読み。
①「がいしゅういっしょく」相手をたやすく打ち負かすこと。
②「ふとうふくつ」どんなことにもくじけない。
③「たりきほんがん」他人任せ。
④「ふげんじっこう」文句を言わず黙々とやること。
⑤「しんぼうえんりょ」先まで考えた深いはかりごと。正しい。
36.国語☆
対義語の組み合わせ。
①壮健と屈強 壮健の対義語は病弱。屈強の対義語は脆弱。
②一般と全般 一般の対義語は特殊。全般の対義語は一端。
③供給と配布 供給の対義語は需要。配布の対義語は回収?
④平易と単純 平易の対義語は難解。単純の対義語は複雑。
⑤集中と分散 正しい。
自然科学
やや難しい。地学の代わりに数学が出題されるのが特徴。
37.数学☆
3桁の自然数で、3でも5でも割り切れない個数。
逆に、3で割り切れる数、5で割り切れる数を900(100~999)から差し引く。
3の倍数(3で割り切れる数)
999÷3=333個 2桁までのものを差し引く99÷3=33個
333-33=300個
5の倍数(5で割り切れる数)
999÷5=199個 2桁までのものを差し引く99÷5=19
199-19=180個
15の倍数(3でも5でも割り切れる数)
66-6=60個は重複して引いているので戻してあげる。
よって
900-300-180+60=480個
こたえ④
38.数学☆☆
3辺と1つの角度だけわかっている三角形の方程式。
三角形のイラストを描いて、余弦定理を用いて、二次方程式を解く。
AB=χ ※辺cとする
BC=(χ+2) ※辺aとする
CA=(χ+1) ※辺bとする
a²=b²+c²-2・b・c・cosAとなるので
cos120°=-cos60°=-0.5より
(χ+2)²=(χ+1)²+χ²-2χ(χ+1)・-0.5
χ²+4χ+4=χ²+2χ+1+χ²+χ²+χ
-2χ²+χ+3=0
χ²-1/2χ-3/2=0
(χ+1)(χ-3/2)=0
χ=-1 と 3/2 ※ただしχ=-1だと辺CAがなくなり不適。
こたえ③
39.数学☆☆
2次関数の平行移動。
y=aχ²+bχ+c をχ軸方向に2移動、y軸方向に3移動なので
y+3=a(χ-2)²+b(χ-2)+c
これをχ軸についてひっくりかえすので、上下逆になり・・・
-(y+3)=a(χ-2)²+b(χ-2)+c
-y=a(χ-2)²+b(χ-2)+c+3
y=-a(χ-2)²-b(χ-2)-c-3
y=-a(χ²-4χ+4)-bχ+2b-c-3
y=-aχ²+4aχ-4a-bχ+2b-c-3
y=-aχ²+(4a-b)χ-4a+2b-c-3
これがy=2χ²-3χ-1になったらしいので
a=-2
(4a-b)=-3より
(-8-b)=-3
b=-5
-4a+2b-c-3=-1
8-10-c-3=-1
-c=4
c=-4
abcをすべて足すと、-11
こたえ⑤
40.物理☆☆
電磁気について。知識がなくてもなんとなくわかる。
①引力と斥力が逆。
②異符号の電荷がひきつけられる。
③直列接続の並列接続の電流と電圧について。正しい。
④常磁性体と反磁性体が逆。
⑤誘導電流が作る磁場は磁束の変化に逆らう方向に生じる。
41.物理☆☆
熱力学について。不正解の選択肢がややマニアック。とりわけ③はひっかかりそう。
①ボイル・シャルルの法則の説明。正しい。
②セルシウス温度-絶対温度=-273
③熱力学第一法則の式はあっているが、Wは気体が外部に行う仕事なのでまちがい。
④理想気体ならば気体の種類のよらずマイヤーの関係式(低圧比熱-定積比熱=気体定数)が成り立つ。
⑤第一種永久機関(外部からエネルギーを与えなくても仕事をする=無からエネルギーを生み出す)ではなく第二種永久機関(外部のエネルギーがすべて仕事をする)の説明。
42.化学☆☆
化学反応式の計算。
モル比は化学反応式の各係数に対応することに注意。
亜鉛は1モルで65gなので、6.5gでは0.1モル。
よって、化学反応式の係数より
亜鉛:0.1モル
塩酸:0.2モル
塩化亜鉛:0.1モル
水素:0.1モル
とすべて1/10となる。
よって、気体の基準体積も22.4ℓではなく2.24ℓになる。
しかし、今回使用した塩酸は
濃さ(モル濃度)が1Lあたり0.5モル
それが200mLあるので、0.1モル
よって、本来0.2モル必要な塩酸が半分しかないことが判る。
こたえは②
発生する水素も半分になるため。
43.化学☆
イオン結晶について。
①イオン結晶が電解質であることの説明。正しい。
②結合の強さは共有結合にはかなわない。
③展性や延性はない。おっかける。
④融点や沸点が高いためムリ。
⑤塩化カルシウムや硫黄、ルビー、サファイアは有色。
44.生物☆
血糖濃度について。易しい。
①血糖濃度は血液中に含まれるグルコースの濃度。
②正しい。
③グルカゴンはランゲルハンス島α細胞。
④アドレナリンは副腎髄質。
⑤糖尿病は血糖値が慢性的に高いと診断される。
45.生物☆☆
近年頻出のバイオーム。
①亜熱帯多雨林の説明。正しい。アコウは別名絞め殺しの木と呼ばれている。
②照葉樹はシイやカシ。ドングリを作るタイプの木。オリーブは硬葉樹。
③夏緑樹はブナ、ミズナラ、カエデ。
④針葉樹はマツやスギなど。
⑤森林限界の2500mを超えると高山。それ以下は亜高山、山地、丘陵。
昨年度から国家一般と日程をかぶせてきたので、どちらかしか受験できなくなった。
難易度は易しすぎず、難しすぎずといった感じ。
データ
全45題 時間は120分
試験問題持ち帰り可能。※解答は公式サイトにアップロード(解説はなし)
星の数は難易度。
☆:易しい。小中学生レベル。
☆☆:普通。高校生レベル。
☆☆☆:難しい。大学入試~大学生レベル。
文章理解
非常に易しい。後半の知識問題がやや難しいので、ここで点数を稼ぎたい。
今年のチョイスはまあまあの面白さだった。
1.内容把握☆
メディアという言葉は様々な意味で使われているよというだけの内容。
こたえは③
2.内容把握☆
美術史についての文章。洞窟壁画などの為政者が権威を示すための美術を不動産美術、15世紀以降のポータブルな流通可能な作品を動産美術と定義している。
選択肢が簡単すぎる。こたえは⑤
3.内容把握☆☆
多数決というシステムに従順で、受動的に選挙で投票している人は、主体的な主権者といえないのではないかといった内容。
本文に合致する選択肢は他にもあるが、要旨として最も妥当なのは⑤
4.空欄補充☆
ヒトは基本的に理性ではなく情動によって行動しているという内容。
こたえは②
5.文章整序☆
生物の進化について。
ゴリラについて書かれている箇所のD→Cを持っているのは①か③か⑤
また、Eの「彼」とはゴリラのシルバーバックのことなので、D→C→Eで確定。
これで①か③
また、Aの「だから」はBの「すべての生命は同じ祖先でつながっている」を受けているので、こたえは①
英語
文章は短く、たいへん易しい。わたしでもできる。
6.英文の内容把握☆
魚にまぶたはないが、常に起きているわけではなく、人間のように寝ているよという内容。
①魚も寝る。
②魚は目を閉じられない。
③流れの静かな穏やかな場所で休む。
④正しい。
⑤だから魚は目を閉じられないって!
7.英文の空欄補充☆
たった3行の会話文。
A:マリリン、(わたしは)マサコです。
B:はい、マサコ!お会いできてうれしいわ。
C:すいませんが、あなたの名前を聞き取れませんでした。
こたえは③
8.英語☆
9月は英語でセプテンバー。
こたえは⑤
判断推理
スタンダードな難易度。
9.論理☆
対偶を作ればいいだけ。
ア:数〇→理〇 理×→数×
イ:社〇→理× 理〇→社×
ウ:数×→英× 英〇→数〇
エ:国〇→英〇 英×→国×
つなげてみると
国〇→英〇→数〇→理〇→社×
こたえは③
10.対応☆
Aの選んだ球技がすぐに確定する。
AとBが選んだのがラグビーか、バスケかで場合分け。

こちらの表はOK!

BとCが野球とバスケをともに選んでいるため、こっちはダメ。
こたえ②Bはラグビーを選んだ。
11.順序☆
仕事が遅い人は時間が大きい。
A:仕事最も遅い=時間大きい
E:仕事最も早い=時間小さい
A-E=20
A-C=11
B-E=13
C=28※5人の平均
28×5=140が全ての時間。
A=39
B=32
C=28
E=19
計118
140-118=22=D!
こたえ③CとDの差6はDとEの差3の2倍。
12.数量☆
5つの箱A~Eにはそれぞれ1,2,3,4,5枚のコインが入っている。
A>B ※A≠1
E>C ※E≠1
A=D+E ※Aは3以上
A=3とすると、D=1、E=2
ただし、A>Bなので無理。
A=4とすると、D=1、E=3、B=2、E=5
A=5とすると、D=2、E=3、B=4、C=1※E>Cのため
E=2、D=3、B=4、C=1
E=2、D=3、C=1、B=4
D=1、E=4、B=3、C=2
D=1、E=4、B=2、C=3
よって、可能なパターンは6通り。
こたえ②
13.平面構成☆
直角三角形の個数。
小×12
中×12
横長×6
半分×4
特大×2
合計④36個
14.平面構成☆
平面パズル。ほとんど同じ問題が問題集にある。
こたえ③
数的推理
約数・倍数、流水算、幾何学、場合の数など、代表的な問題をバランスよく出題。
15.約数・倍数☆
AとBは5:7で280の公約数。
5χ×7χ=280
35χ=280
χ=8
よってA=40、B=56
こたえ④
16.流水算☆
上り(減速)も下り(加速)も川の道のりは変わらない。
船の速さをχ、川の速さをyとする。
下りの道のり=上りの道のり
20分×(χ+y)=30分×(χ-y)
20χ+20y=30χ-30y
-10χ=-50y
χ=5y
つまり、船の速度は川の速度の5倍
下りの速度は、川の速度の6倍なので、川の流れだけで下ると、速度は1/6
よって、時間が6倍となる。
こたえ③120分
17.平面図形☆
たのしい数字合わせ。
P:12cm² 3×4
Q:36cm² 9×4
R:24cm² 3×8
なので
S:9×8
よってすべての辺を足すと、9+9+8+8=34cm
こたえ③
18.場合の数☆☆
わりとめんどうくさい。
1円と50円と100円が2枚ずつあるので、重複をはじけば50円刻みで考えると判りやすい。
1円 2円
50円 51円 52円
100円 101円 102円
150円 151円 152円
200円 201円 202円
250円 251円 252円
300円 301円 302円
こたえ③20通り
資料解釈
4問も出るのを忘れてた。が、特別区の100倍易しい。こういうのでいいんだよ。
19.表☆
これは易しい。
①18年の全項目を足せばよい。50%は超えないのはすぐにわかる。
②16年→20年なので、20年÷16年で計算
コーヒー豆:1.1倍
カカオ豆:1.28倍
茶:1.17倍
よって正しい。
③16年のみ。
④どう考えても3000千トンくらいしか多くない。
⑤指数は106なのでダメ。
20.表☆
①世界総計の30%を出せばいいから、0.3をかけると18年がダメ。
②10000千台を超える端数を足していくと、下回らない。
③5646×0.6=3387なので、60%未満。正しい。
④いけそうだが、21年がぎりぎりダメ。
⑤対前年減少“数”なので、日本ではなく中国。
21.グラフ☆
東京消防庁らしい火災の統計グラフ。
①グラフの高さを100で割って4倍する。すべて下回るので正しい。
②4053×0.8=3242なのでダメ。
③これも減少“数”なので、車両火災-119、林野火災-152なのでダメ。
④絶対違う。
⑤グラフの長さ的に16年が違うことは瞭然。
22.表&グラフ☆
①18年が怪しい(他は絶対違う)。1138305×0.63=717132なのでダメ。
②16年のアメリカは258729なので、その1.15倍は297538。ダメ。
③怪しい年(16年、17年、20年)だけを計算。
16年は124711、17年は85469、20年は99791。正しい。
④19年の日本99287の6倍は595725なのでダメ。ロシアは540800。
⑤17年アメリカ461090の50%は230545なのでダメ。18年アメリカは265225。
社会科学
スタンダードな難易度。
23.政治☆☆
基本的人権についてだが、ちょっとへんてこな問題。
ただし、不正解の選択肢が判りやすいので選びやすい。
①日本国憲法に法律の留保はない。
②公務員試験で初めて見た、栄典制度の説明。紫綬褒章など。正しい。
③投票の選択に私的な責任を問われるわけがない。
④憲法26条は「その能力に応じて」等しく教育を受ける権利を有する。
⑤団体行動権ももちろん保障される。
24.政治☆
憲法改正の発議は内閣ではなく国会。(憲法96条1項)
こたえ④
25.経済☆☆
①公共財は非競合性や非排除性を「持つ」。
②財政投融資は国債の一種である財投債で資金を調達する。
③ビルトインスタビライザーの説明。正しい。
④納入者と負担者が逆。
⑤水平的公平ではなく垂直的公平。
26.社会☆
日本の環境問題。
①汚染者負担の原則の説明。正しい。
②環境アセスメント法(97年公布)があるのでまちがい。
③3Rに特に優先順位はない。
④四台公害訴訟で原告側は勝訴。関係法令が見直され、賠償金も出た(しかし低かった)。
⑤環境基本法は93年に公布されたので、11年の東日本震災を受けて出来てはいない。
27.社会☆
育児休暇制度について。
A:子どもが原則1歳まで。
B:正しい。
C:正しい。
D:育休手当は会社ではなくハローワークから支給される。
人文科学
歴史の問題は経緯を時系列に並べる問題が多く、うろ覚えだとかなり厳しい。
28.西洋史☆☆
ロシア革命の流れの順番合わせ。
第一次世界大戦中に第二革命が成功し、ドイツと単独講和をして、戦後にソ連を成立させている。
C:サラエボ事件(1914)
B:第二ロシア革命(1917)
E:ブレスト=リトフスク条約(1918)
A:ソ連成立(1922)
D:スターリンが五か年計画スタート(1928)
こたえは④
29.西洋史☆
世界恐慌についての正誤問題。
ア:アメリカのニューディール政策の説明。正しい。
イ:マクドナルド内閣はフランスではなくイギリスの労働党政権。
ウ:ソ連の五か年計画は世界恐慌の影響を受けなかった。
エ:ヒトラーの公共事業の説明。正しい。
こたえは②
30.日本史☆
明治時代後半の流れの順番合わせ。
C:日清戦争(1894)
B:三国干渉(1895)※日清戦争で得た遼東半島を手放すことに。
E:日英同盟(1902)南下政策をするロシアを警戒。
A:日露戦争(1904)
D:韓国併合(1910)
こたえは③
31.日本史☆☆※
太平洋戦争についての記述。選択肢②が史観によっては正しい気もしないでもない。
この時代を出題するのはどうかと思う。
①ミッドウェー海戦に日本は敗北している。
②大東亜共栄圏はアジアエリアの白人植民地の開放が立て前。微妙。
③女子も勤労動員にかけられた。
④45年3月東京大空襲→4月沖縄戦→8月原子爆弾。正しい。
⑤ポツダム宣言を直ちに受諾していれば原爆は落とされなかった。
32.地理☆☆
エネルギーや鉱物について。
①西アジア(アラブ)の産油国はOPECではなくOAPEC。他は正しい。
②天然ガスは石油に比べて二酸化炭素排出量が少ないが、メタンガスの形で輸送中に漏れたりもするため、近年の発表では温暖化抑制効果は思ったよりも低いと言われている。
③世界に占める原子力発電の割合は3割弱。
④正しい。
⑤レアメタルは高価な金属ではなく、希少な金属のこと。プラチナやリチウム、コバルトなど。
33.地理☆
中国について。
ア:経済特区の記述。正しい。
イ:ウイグル族に対するジェノサイドの記述。正しい。
ウ:一人っ子政策の効果は抜群で、日本以上の少子高齢化になるとも言われている。
こたえは①
34.国語☆
漢字の書き。
①「異常」気象
②校庭を「開放」
③留学生と「交歓」正しい。
④「暗証」番号
⑤値段の「見当」
35.国語☆☆
四字熟語の読み。
①「がいしゅういっしょく」相手をたやすく打ち負かすこと。
②「ふとうふくつ」どんなことにもくじけない。
③「たりきほんがん」他人任せ。
④「ふげんじっこう」文句を言わず黙々とやること。
⑤「しんぼうえんりょ」先まで考えた深いはかりごと。正しい。
36.国語☆
対義語の組み合わせ。
①壮健と屈強 壮健の対義語は病弱。屈強の対義語は脆弱。
②一般と全般 一般の対義語は特殊。全般の対義語は一端。
③供給と配布 供給の対義語は需要。配布の対義語は回収?
④平易と単純 平易の対義語は難解。単純の対義語は複雑。
⑤集中と分散 正しい。
自然科学
やや難しい。地学の代わりに数学が出題されるのが特徴。
37.数学☆
3桁の自然数で、3でも5でも割り切れない個数。
逆に、3で割り切れる数、5で割り切れる数を900(100~999)から差し引く。
3の倍数(3で割り切れる数)
999÷3=333個 2桁までのものを差し引く99÷3=33個
333-33=300個
5の倍数(5で割り切れる数)
999÷5=199個 2桁までのものを差し引く99÷5=19
199-19=180個
15の倍数(3でも5でも割り切れる数)
66-6=60個は重複して引いているので戻してあげる。
よって
900-300-180+60=480個
こたえ④
38.数学☆☆
3辺と1つの角度だけわかっている三角形の方程式。
三角形のイラストを描いて、余弦定理を用いて、二次方程式を解く。
AB=χ ※辺cとする
BC=(χ+2) ※辺aとする
CA=(χ+1) ※辺bとする
a²=b²+c²-2・b・c・cosAとなるので
cos120°=-cos60°=-0.5より
(χ+2)²=(χ+1)²+χ²-2χ(χ+1)・-0.5
χ²+4χ+4=χ²+2χ+1+χ²+χ²+χ
-2χ²+χ+3=0
χ²-1/2χ-3/2=0
(χ+1)(χ-3/2)=0
χ=-1 と 3/2 ※ただしχ=-1だと辺CAがなくなり不適。
こたえ③
39.数学☆☆
2次関数の平行移動。
y=aχ²+bχ+c をχ軸方向に2移動、y軸方向に3移動なので
y+3=a(χ-2)²+b(χ-2)+c
これをχ軸についてひっくりかえすので、上下逆になり・・・
-(y+3)=a(χ-2)²+b(χ-2)+c
-y=a(χ-2)²+b(χ-2)+c+3
y=-a(χ-2)²-b(χ-2)-c-3
y=-a(χ²-4χ+4)-bχ+2b-c-3
y=-aχ²+4aχ-4a-bχ+2b-c-3
y=-aχ²+(4a-b)χ-4a+2b-c-3
これがy=2χ²-3χ-1になったらしいので
a=-2
(4a-b)=-3より
(-8-b)=-3
b=-5
-4a+2b-c-3=-1
8-10-c-3=-1
-c=4
c=-4
abcをすべて足すと、-11
こたえ⑤
40.物理☆☆
電磁気について。知識がなくてもなんとなくわかる。
①引力と斥力が逆。
②異符号の電荷がひきつけられる。
③直列接続の並列接続の電流と電圧について。正しい。
④常磁性体と反磁性体が逆。
⑤誘導電流が作る磁場は磁束の変化に逆らう方向に生じる。
41.物理☆☆
熱力学について。不正解の選択肢がややマニアック。とりわけ③はひっかかりそう。
①ボイル・シャルルの法則の説明。正しい。
②セルシウス温度-絶対温度=-273
③熱力学第一法則の式はあっているが、Wは気体が外部に行う仕事なのでまちがい。
④理想気体ならば気体の種類のよらずマイヤーの関係式(低圧比熱-定積比熱=気体定数)が成り立つ。
⑤第一種永久機関(外部からエネルギーを与えなくても仕事をする=無からエネルギーを生み出す)ではなく第二種永久機関(外部のエネルギーがすべて仕事をする)の説明。
42.化学☆☆
化学反応式の計算。
モル比は化学反応式の各係数に対応することに注意。
亜鉛は1モルで65gなので、6.5gでは0.1モル。
よって、化学反応式の係数より
亜鉛:0.1モル
塩酸:0.2モル
塩化亜鉛:0.1モル
水素:0.1モル
とすべて1/10となる。
よって、気体の基準体積も22.4ℓではなく2.24ℓになる。
しかし、今回使用した塩酸は
濃さ(モル濃度)が1Lあたり0.5モル
それが200mLあるので、0.1モル
よって、本来0.2モル必要な塩酸が半分しかないことが判る。
こたえは②
発生する水素も半分になるため。
43.化学☆
イオン結晶について。
①イオン結晶が電解質であることの説明。正しい。
②結合の強さは共有結合にはかなわない。
③展性や延性はない。おっかける。
④融点や沸点が高いためムリ。
⑤塩化カルシウムや硫黄、ルビー、サファイアは有色。
44.生物☆
血糖濃度について。易しい。
①血糖濃度は血液中に含まれるグルコースの濃度。
②正しい。
③グルカゴンはランゲルハンス島α細胞。
④アドレナリンは副腎髄質。
⑤糖尿病は血糖値が慢性的に高いと診断される。
45.生物☆☆
近年頻出のバイオーム。
①亜熱帯多雨林の説明。正しい。アコウは別名絞め殺しの木と呼ばれている。
②照葉樹はシイやカシ。ドングリを作るタイプの木。オリーブは硬葉樹。
③夏緑樹はブナ、ミズナラ、カエデ。
④針葉樹はマツやスギなど。
⑤森林限界の2500mを超えると高山。それ以下は亜高山、山地、丘陵。
R5年度特別区(東京23区)職員Ⅲ類採用試験について
2023-09-12 19:24:45 (2 years ago)
-
カテゴリタグ:
- 資格試験
全体的な感想
昨年よりもかなり易しいが(日本史除く)、資料解釈だけがとんでもなく面倒。
試験時間が限られているので、資料解釈はすべて後回しが良い。
データ
全50問(解答は45問) 時間は2時間
必答問題:28問
選択問題:22題から17問を選択。※5問は捨てられる。
試験問題持ち帰り可能。
星の数は難易度。
☆:易しい。小中学生レベル。
☆☆:普通。高校生レベル。
☆☆☆:難しい。大学入試~大学生レベル。
※:判定不能。悪問や、出題ミスなど。
文章理解
昨年よりも現代文は易しいので、毎年だけどここで得点を稼ぎたい。
1.内容把握☆
簡単な文章の主旨を選ぶ問題だが、
③つぼみはひとりでに花開くことはない
か
④つぼみが花開くためには刺激が必要である
でちょっと迷う。
おそらく④だと思う。
2.内容把握☆
対話においては、話す準備に意識が行きがちだが、実は聞く準備も努力が要るし、責任も重いという内容。
②も捨てがたいが(上手い問題提起だと思う)、本文の末にある⑤が要旨なのだろう。
3.文章整序☆
Bの「わりあい早歩きです」はEのウォーキングマシーンでの運動の説明なのでE→Bとなる。その選択肢は④のみ。
4.文章整序☆
もうどう考えてもA→Eなので、この時点で②か③の2択。
「事実」についての考察がB→F→Dと続くので③
5.空欄補充☆
Aに入る語は「現実的」なので①③⑤に絞られる。
Bは「過小評価」で①か③
日本人は理論体系そのものを作ること(革新)は苦手なので、Cは「改良」
よって、こたえは①
6.空欄補充☆
美術評論家についての内容。
Aに「敬称」は入らない。
Bが「瞬発的」なジャッジが入るので、②か④
しかし、Cがどう考えても「対照的」が入るので、②で確定。
英語
7.内容把握☆
①正しい。
②ポール・ジョブズはスティーブ・ジョブズの大学の学費を車の修理で稼いだ。
③ポールが若きスティーブに教えた。
④スティーブが学んだことの内容。
⑤特別な人ではなく一般(ordinary people)の人向け。
8.空欄補充
こたえは④らしい。
9.空欄補充
こたえは⑤らしい。
判断推理
10.勝敗☆☆
6人の総当たり戦なので、試合の数は一人当たり5戦の全15試合。
あと3試合残っているので12試合は終了。
引き分けはないので、12勝と12敗を表に入れていく。
ヒントアより、Aは3勝2敗。
ヒントイより、Bは少なくとも3敗で、うち一回はDとの対戦。
ヒントウより、CとFは全勝。Fは少なくとも4勝。
ヒントエより、Dは1勝4敗。
ヒントオより、EはAに敗北、Bに勝利。
ヒントイとエより、Dの貴重な1勝はBとの試合なので、Dの勝敗はすべて確定。
Fがめちゃくちゃ強いが、Cも0敗なので、C対Fは行われていないことが判る。
そんな感じで、0敗の選手から攻めると以下の表に埋まる。
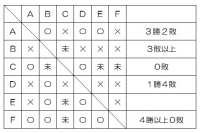
よって、こたえは③
11.暗号☆
特別区は、毎年暗号が出るらしい。
どう考えても「いろはにほへと」だが、「ちりぬるを」以降がうろ覚えで出てこない。
しかし、マークを替えて「いろはにほへと」で循環しているっぽいので助かった。
□と〇だけ、アルファベットと「いろは」が合わないが、逆走させればハマることが判る。

こたえは⑤
12.発言推理☆
全部の発言を正しいとして、順番を並べてしまう。
そして一人ずつ嘘つきだと仮定して、嘘つきになってしまうと、成立しない人物を割り出す。
すべての発言が正しいと、順番は以下のようになる。
C>D>A>B>E
ここで、Dの発言「C>E」が嘘だとすると「E>C」となり
D>A>B>E>Cとなり、Bの発言「C>D」とも矛盾し、1人だけ嘘がつけない。
こたえは④
13.方位☆
北を上とします。
A~Fが縦か横のどちらで並んでいるかがわからないが、ヒントのウでCが東を向いていることが判るため、以下のようになる。
F ←
E ↑
D ←
C →
B ←
A →
こたえ①
14.数量☆
わりとゴリ押せる。
Aは(3n+3)※3つの連続する数字と何かで29を、
Bは4枚で26を、
Cは3枚で13を作らなければならない。
n=1 合計6なので残り23 ダメ
n=2 合計9 残り20 ダメ
n=3 合計12 残り17 ダメ
n=4 合計15 残り14 ダメ
n=5 合計18 残り11 Cが11を持っているため、ダメ
n=6 合計21 残り8 (6,7,8)になるため、8が重複。ダメ。
n=7 合計24 残り5
n=8 合計27 残り2
よって、Aの連続する三枚は、7,8,9か、8,9,10の2通り。
この時点で正解が確定するが、BとCの数字も割り振ってみると
A:7,8,9,5 計29
B:12,13,3,4,6
C:11,10,2,1
A:8,9,10,2 計29
B:12,13,7,5,1
C:11,6,4,3
いずれにせよAには8、Bには13がある。こたえ②
15.位置☆
ヒントエが強い。BはCの下で「時計」を買っている。
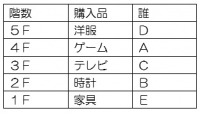
こたえは②
数的処理
16.角度☆
OとAを結んで円の中心から接線に垂線を下ろす。
二等辺三角形OCAより中心角は144°
∠AOB=36°
直角三角形OABより、∠ABC=54°
こたえは③
17.数列☆☆☆
初項3に9に4をn回かけた数を足している等比数列。
第8項までの和はすごいことになる。
等比数列の和の公式を使うと、初項3、公比4、項数8なので
3×(4⁸-1)/4-1=65535 ※4の8乗が鬼畜!
17,24,31,38・・・の等差数列は
17+(7×39)=290
65535+290=65825
こたえは④
18.旅人算☆
二人の速さの比はA:B=4:3
つまり、2100mのコースを、AとBで毎回4:3に分け合う。
Aは1200m、Bは900m走るとすれ違う。
スタート地点からの距離は時計回りで求めるので、時計回りに走っているAさんで考える。
4回目のすれ違いなので1200×4=4800m
4800-2100-2100=600mの地点。
こたえ②
19.確率☆
3個を同時に取り出すので、順番は関係ない。
すべて赤:5・4・3/3・2・1=10パターン
すべて白:3・2・1/3・2・1=1パターン
すべて黄:4・3・2/3・2・1=4パターン
合計は15パターン
赤白黄:5・3・4=60パターン
こたえは④の4倍。
20.方程式☆
全距離をχkmとする。
1日目:(χ/3)-8
2日目:{χ-(χ/3-8)}÷2+50
3日目:(χ/4)-2
これをすべて足すとχなので、方程式を解く。
χ=528km
こたえ①
資料解釈
どれも計算が面倒。概算で正解が選べないのが難しい。
21.表☆☆
選択肢が割と際どいので、概数で計算すると危険。
①17年:6876÷55519=0.12
16年:0.13 まちがい。
②イタリア:1.17 スペイン:1.16 正しい。
③フランスの指数は104なのでまちがい。
④輸入数量の合計を5で割って検証すると、2020年がダメ。
⑤18年がダメ。
22.表☆☆☆
面倒な対前年比。
①18年を100として計算していくと、106になるので正しい。
②農産物の増加率9%、林産物の増加率28%なので、林産物は農産物の3倍を下回る。
③農産物の②の計算をそのまま使う。
17年:100 18年:103 19年:102 20年:96.5 21年:109
なので最も多いのは21年。
④水産物 18年:100 19年:97.2 20年:81 21年:89.9!
90%をぎりぎり超えない!
⑤具体的な輸入額は不明!
23.棒グラフ☆☆
①令和3年だけ3.3倍を上回ってしまうのでまちがい。
②H30→R1:1493 R1→R2:19684 R2→R3:49309
すべて足して3で割ると234954kLなのでまちがい。
③約96.4なのでまちがい。
④飲用牛乳は増えているので問題外。残りはR3÷R2で求める。
乳飲料は95%、発酵乳は97%、乳酸菌飲料は96%なので、正しい。
⑤発酵乳:30276 乳酸菌飲料:1256×33=41448 まちがい。
24.円グラフ☆☆
全体の割合から具体的な値を求めてから計算するのが面倒。
①21167(H22)÷16796(R2)=1.26なのでまちがい。
②14101(H22)×1.2=16921
15653(R2)なので1.2を下回る。
③3人(R2):9247 4人(R2):6628 5000は上回らない。
④5人以上の減少率:3008÷4043=74%
4人の減少率:6628÷7465=88%
よって3倍より下回る。
⑤5人以上の減少数:4043-3008=1035
3人の減少数:9435-9247=188
よって188×4=752なので、正しい。
判断推理
恒例の第二部、図形問題。
25.正多面体☆
正多面体の辺の数は、1面あたりの辺×面数÷2
正六面体の辺は、面の形が四角刑なので4辺×6面÷2=12本。
正12面体の辺は、面の形が五角形なので5辺×12面÷2=30本。
正多面体の頂点の数は、1面当たりの角の数×面数÷頂点に集まる辺の数
正八面体の頂点は6つなので、すべて足すと③48
26.平面構成☆
面積100cm²の茶の折り紙から攻める。
12分割中の2区画が赤で隠れるので、1区画10cm²と判る。
よって、緑の折り紙の面積は30cm²
こたえは③
27.立体図形☆
6√2の辺が2つ。
3√2の辺が4つ。
3√2の辺が1つ。
こたえは④
28.軌跡☆
とんでもなく易しい。
こたえは⑤
ココから選択問題
問題によって難易度がまちまちなので、ひととおり目を通して、易しそうな問題だけを選ぶ。
社会科学
すべて易しい。ここでポイントを稼ぐ。
29.政治☆
日本国憲法について。
①欽定憲法ではなく民定憲法。
②軟性憲法ではなく硬性憲法。
③マッカーサー草案を受けて作成。
④法律の留保はなし。
⑤正しい。
30.政治☆
裁判所について。 本当に近年この分野がよく出るなあ。
①現在の日本に行政裁判所はない。
②知的財産高等裁判所は東京高裁の支部なので、全国8か所のすべての高等裁判所には設置されていない。
③違憲法令審査権は下級裁判所にも与えられている。
④最高裁判所裁判官の国民審査は、その人が最高裁判所裁判官に任命されて初めて行われる衆議院選挙の際に実施され、その後は最初の国民審査から10年経過して初めて行われる衆議院選挙の際に再び国民審査が行われる。つまり、参議院選挙の際には行われない。
⑤検察審査会の説明。正しい。
31.政治☆
日本の選挙制度について。小中学校レベル。
①衆議院選挙の説明。正しい。
②参議院選挙でも比例区はある。
③比例代表制は少数派政党にも議席獲得のチャンスがある。
④小選挙区は死票が多い。
⑤一票の格差について最高裁の違憲判決が出ている。
32.経済☆
国民所得について。
①国民総所得、国民純生産、国民所得の説明。正しい。
②生産、分配、支出の金額は等しい(三面等価の原則)。
③国富に対外資産は含まれる。
④ジュグラーの波ではなく、コンドラチェフの波。
⑤コンドラチェフの波ではなく、ジュグラーの波。
33.心理学☆☆
今年は資源の問題ではなくなった。
①ヤマアラシのジレンマはルソーではなくショーペンハウアー。説明も間違い。
②ホリングワースではなく、エリクソン。
③マージナルマンの説明。正しい。
④発達課題はマズローではなく、ハヴィガースト。
⑤フロイトではなくエリクソン。
人文科学
日本史でとんでもなくマニアックな奴が登場。
34.日本史☆☆☆
今年は飛鳥時代の文化。毎年文化っぽい?
①正しい。
②飛鳥寺は蘇我入鹿ではなく蘇我馬子。
③高句麗からやってきた曇徴(どんちょう)は製紙技術や絵の具、墨の作成の専門家だった。マニアック!三経義疏(さんぎょうぎしょ)は聖徳太子が著した。
④百済観音像の作者は不明。
⑤百済からやってきた観勒(かんろく)は日本に天文、暦本、陰陽道を伝えた。
35.日本史☆☆
日本の近代化について。
①幕末の日本の最大の輸出品は生糸。
②臥雲辰致は織機ではなく国産紡績機の発明者。
③座繰製糸が富岡製糸場などの機械製糸にパワーアップ。
④東海道本線は政府が敷いた最古の鉄道路線。
⑤正しい。
36.西洋史☆
宗教改革について。
①贖宥状ビジネスを行ったのはカール5世ではなくレオ10世。カール5世は教皇ではなく、ハプスブルグ家全盛期の神聖ローマ帝国の皇帝。
②ドイツ農民戦争は教皇ではなく、皇帝軍と戦った。
③カルヴァンは司教(ルターが支持)ではなく長老が協会の運営を行うべきだとした。
④エリザベス1世は英国国教会を廃止していない。
⑤正しい。
37.東洋史☆☆
不正解の選択肢の記述がめちゃマニアック。
①北宋と南宋が逆。
②形勢戸は唐代の新興貴族。中国版ユンカー的な大地主。
③正しい。
④鎮は宋代の農村の市場中心地のこと。行は商人の同業組合
⑤訓詁学が儒教の難しい用語を解説する学問。
38.地理☆
ケッペンの気候区分について。
①高山気候はケッペンの気候区分にはない。
②熱帯にステップはない。
③西岸海洋性気候の説明。
④正しい。
⑤寒帯は最も暖かい月の気温が10℃未満。
39.倫理☆
西洋哲学。
①ベーコンの説明。正しい。
②ヒュームではなくベーコンの内容。
③自我と物体の説明が逆。
④ライプニッツではなくスピノザの説明。
⑤スピノザではなくライプニッツの説明。
自然科学
物理は毎年2問とも計算みたい。
40.物理☆
仕事率。単位変換はしなくていい。
30kg × 9.8m/s² × 20m = 約6000Jの仕事を10秒で行うので
1秒あたりの仕事率は10で割って600W
答えは④
41.物理☆☆
電力損失の計算問題。ちょっとわかりにくい。
電力が1000W、電圧が200Vなので電流は5A。
W=A²×Ωなので
5²A×2Ω=50
よって電力損失は50W。
電力損失は電圧を上げると下がる(電流が下がりジュール熱が抑えられるため)。
W=V²/Ωより、電力損失は電圧の2乗に比例。
よって、電圧を5倍にすると、電力損失は1/25に抑えられる。
こたえ⑤
42.化学☆
中和滴定。価数と濃度と体積の積を合わせればよい。
濃度不明の塩酸・・・1価×χmol/L×10mL
水酸化カルシウム・・・2価×0.20mol/L×15mL
上の二つの答えを等式でつないで方程式を解く。
χ=0.60mol/L
こたえ⑤
43.化学☆
化合物や同素体について。覚えるだけの問題。易しい。
こたえは④
44.生物☆
遺伝情報とタンパク質の合成。
A:正しい。
B:DNAからRNAが転写される。
C:正しい。
D:DNA→RNA→タンパク質の順番。
こたえは②
45.生物☆
肝臓について。
①腎臓の説明。
②アルブミンを分解ではなく合成。
③正しい。
④アンモニアを尿素に変える。
⑤ホルモンの一種バソプレシンの命令で水を飲むことで塩分濃度を下げる。
46.地学☆
火山について。
A:正しい。
B:粘性が逆。
C:正しい。
D:楯状火山ではなく成層火山。
こたえは②
文学・芸術
47.漢字の読み☆
A:あんちゅうもさく
B:いちじつせんしゅう
C:うんさんむしょう
D:えいこせいすい
E:おかめはちもく
こたえは③
48.ことわざ・慣用句☆
A:どちらも肝が入る。
B:青天白日 清濁併せ呑む
C:どちらも竹が入る
D:森羅万象 神出鬼没
こたえは②
49.古典☆☆
出典は『枕草子』無名といふ琵琶
①「まろ」は一人称。「あなたのところに」ではなく「私のところに」
②正しい。
③「淑景舎の笛が欲しい僧侶の隆円は何とか答えさせようと何回もお聞きになる」
④あまりに笛が欲しい僧侶がしつこいので、中宮が代わりに「笛を交換したくないと思っています」と答えた。
⑤僧侶は笛の名前を知らなかった。
50.日本音楽☆☆☆
筝曲の有名な人物を選ぶ。
八橋はもともと琴の形をしたお菓子であるということを知っていれば判る。
でも、最近は生八橋が主流なので、苦戦は否めない。
こたえ①
昨年よりもかなり易しいが(日本史除く)、資料解釈だけがとんでもなく面倒。
試験時間が限られているので、資料解釈はすべて後回しが良い。
データ
全50問(解答は45問) 時間は2時間
必答問題:28問
選択問題:22題から17問を選択。※5問は捨てられる。
試験問題持ち帰り可能。
星の数は難易度。
☆:易しい。小中学生レベル。
☆☆:普通。高校生レベル。
☆☆☆:難しい。大学入試~大学生レベル。
※:判定不能。悪問や、出題ミスなど。
文章理解
昨年よりも現代文は易しいので、毎年だけどここで得点を稼ぎたい。
1.内容把握☆
簡単な文章の主旨を選ぶ問題だが、
③つぼみはひとりでに花開くことはない
か
④つぼみが花開くためには刺激が必要である
でちょっと迷う。
おそらく④だと思う。
2.内容把握☆
対話においては、話す準備に意識が行きがちだが、実は聞く準備も努力が要るし、責任も重いという内容。
②も捨てがたいが(上手い問題提起だと思う)、本文の末にある⑤が要旨なのだろう。
3.文章整序☆
Bの「わりあい早歩きです」はEのウォーキングマシーンでの運動の説明なのでE→Bとなる。その選択肢は④のみ。
4.文章整序☆
もうどう考えてもA→Eなので、この時点で②か③の2択。
「事実」についての考察がB→F→Dと続くので③
5.空欄補充☆
Aに入る語は「現実的」なので①③⑤に絞られる。
Bは「過小評価」で①か③
日本人は理論体系そのものを作ること(革新)は苦手なので、Cは「改良」
よって、こたえは①
6.空欄補充☆
美術評論家についての内容。
Aに「敬称」は入らない。
Bが「瞬発的」なジャッジが入るので、②か④
しかし、Cがどう考えても「対照的」が入るので、②で確定。
英語
7.内容把握☆
①正しい。
②ポール・ジョブズはスティーブ・ジョブズの大学の学費を車の修理で稼いだ。
③ポールが若きスティーブに教えた。
④スティーブが学んだことの内容。
⑤特別な人ではなく一般(ordinary people)の人向け。
8.空欄補充
こたえは④らしい。
9.空欄補充
こたえは⑤らしい。
判断推理
10.勝敗☆☆
6人の総当たり戦なので、試合の数は一人当たり5戦の全15試合。
あと3試合残っているので12試合は終了。
引き分けはないので、12勝と12敗を表に入れていく。
ヒントアより、Aは3勝2敗。
ヒントイより、Bは少なくとも3敗で、うち一回はDとの対戦。
ヒントウより、CとFは全勝。Fは少なくとも4勝。
ヒントエより、Dは1勝4敗。
ヒントオより、EはAに敗北、Bに勝利。
ヒントイとエより、Dの貴重な1勝はBとの試合なので、Dの勝敗はすべて確定。
Fがめちゃくちゃ強いが、Cも0敗なので、C対Fは行われていないことが判る。
そんな感じで、0敗の選手から攻めると以下の表に埋まる。

よって、こたえは③
11.暗号☆
特別区は、毎年暗号が出るらしい。
どう考えても「いろはにほへと」だが、「ちりぬるを」以降がうろ覚えで出てこない。
しかし、マークを替えて「いろはにほへと」で循環しているっぽいので助かった。
□と〇だけ、アルファベットと「いろは」が合わないが、逆走させればハマることが判る。

こたえは⑤
12.発言推理☆
全部の発言を正しいとして、順番を並べてしまう。
そして一人ずつ嘘つきだと仮定して、嘘つきになってしまうと、成立しない人物を割り出す。
すべての発言が正しいと、順番は以下のようになる。
C>D>A>B>E
ここで、Dの発言「C>E」が嘘だとすると「E>C」となり
D>A>B>E>Cとなり、Bの発言「C>D」とも矛盾し、1人だけ嘘がつけない。
こたえは④
13.方位☆
北を上とします。
A~Fが縦か横のどちらで並んでいるかがわからないが、ヒントのウでCが東を向いていることが判るため、以下のようになる。
F ←
E ↑
D ←
C →
B ←
A →
こたえ①
14.数量☆
わりとゴリ押せる。
Aは(3n+3)※3つの連続する数字と何かで29を、
Bは4枚で26を、
Cは3枚で13を作らなければならない。
n=1 合計6なので残り23 ダメ
n=2 合計9 残り20 ダメ
n=3 合計12 残り17 ダメ
n=4 合計15 残り14 ダメ
n=5 合計18 残り11 Cが11を持っているため、ダメ
n=6 合計21 残り8 (6,7,8)になるため、8が重複。ダメ。
n=7 合計24 残り5
n=8 合計27 残り2
よって、Aの連続する三枚は、7,8,9か、8,9,10の2通り。
この時点で正解が確定するが、BとCの数字も割り振ってみると
A:7,8,9,5 計29
B:12,13,3,4,6
C:11,10,2,1
A:8,9,10,2 計29
B:12,13,7,5,1
C:11,6,4,3
いずれにせよAには8、Bには13がある。こたえ②
15.位置☆
ヒントエが強い。BはCの下で「時計」を買っている。

こたえは②
数的処理
16.角度☆
OとAを結んで円の中心から接線に垂線を下ろす。
二等辺三角形OCAより中心角は144°
∠AOB=36°
直角三角形OABより、∠ABC=54°
こたえは③
17.数列☆☆☆
初項3に9に4をn回かけた数を足している等比数列。
第8項までの和はすごいことになる。
等比数列の和の公式を使うと、初項3、公比4、項数8なので
3×(4⁸-1)/4-1=65535 ※4の8乗が鬼畜!
17,24,31,38・・・の等差数列は
17+(7×39)=290
65535+290=65825
こたえは④
18.旅人算☆
二人の速さの比はA:B=4:3
つまり、2100mのコースを、AとBで毎回4:3に分け合う。
Aは1200m、Bは900m走るとすれ違う。
スタート地点からの距離は時計回りで求めるので、時計回りに走っているAさんで考える。
4回目のすれ違いなので1200×4=4800m
4800-2100-2100=600mの地点。
こたえ②
19.確率☆
3個を同時に取り出すので、順番は関係ない。
すべて赤:5・4・3/3・2・1=10パターン
すべて白:3・2・1/3・2・1=1パターン
すべて黄:4・3・2/3・2・1=4パターン
合計は15パターン
赤白黄:5・3・4=60パターン
こたえは④の4倍。
20.方程式☆
全距離をχkmとする。
1日目:(χ/3)-8
2日目:{χ-(χ/3-8)}÷2+50
3日目:(χ/4)-2
これをすべて足すとχなので、方程式を解く。
χ=528km
こたえ①
資料解釈
どれも計算が面倒。概算で正解が選べないのが難しい。
21.表☆☆
選択肢が割と際どいので、概数で計算すると危険。
①17年:6876÷55519=0.12
16年:0.13 まちがい。
②イタリア:1.17 スペイン:1.16 正しい。
③フランスの指数は104なのでまちがい。
④輸入数量の合計を5で割って検証すると、2020年がダメ。
⑤18年がダメ。
22.表☆☆☆
面倒な対前年比。
①18年を100として計算していくと、106になるので正しい。
②農産物の増加率9%、林産物の増加率28%なので、林産物は農産物の3倍を下回る。
③農産物の②の計算をそのまま使う。
17年:100 18年:103 19年:102 20年:96.5 21年:109
なので最も多いのは21年。
④水産物 18年:100 19年:97.2 20年:81 21年:89.9!
90%をぎりぎり超えない!
⑤具体的な輸入額は不明!
23.棒グラフ☆☆
①令和3年だけ3.3倍を上回ってしまうのでまちがい。
②H30→R1:1493 R1→R2:19684 R2→R3:49309
すべて足して3で割ると234954kLなのでまちがい。
③約96.4なのでまちがい。
④飲用牛乳は増えているので問題外。残りはR3÷R2で求める。
乳飲料は95%、発酵乳は97%、乳酸菌飲料は96%なので、正しい。
⑤発酵乳:30276 乳酸菌飲料:1256×33=41448 まちがい。
24.円グラフ☆☆
全体の割合から具体的な値を求めてから計算するのが面倒。
①21167(H22)÷16796(R2)=1.26なのでまちがい。
②14101(H22)×1.2=16921
15653(R2)なので1.2を下回る。
③3人(R2):9247 4人(R2):6628 5000は上回らない。
④5人以上の減少率:3008÷4043=74%
4人の減少率:6628÷7465=88%
よって3倍より下回る。
⑤5人以上の減少数:4043-3008=1035
3人の減少数:9435-9247=188
よって188×4=752なので、正しい。
判断推理
恒例の第二部、図形問題。
25.正多面体☆
正多面体の辺の数は、1面あたりの辺×面数÷2
正六面体の辺は、面の形が四角刑なので4辺×6面÷2=12本。
正12面体の辺は、面の形が五角形なので5辺×12面÷2=30本。
正多面体の頂点の数は、1面当たりの角の数×面数÷頂点に集まる辺の数
正八面体の頂点は6つなので、すべて足すと③48
26.平面構成☆
面積100cm²の茶の折り紙から攻める。
12分割中の2区画が赤で隠れるので、1区画10cm²と判る。
よって、緑の折り紙の面積は30cm²
こたえは③
27.立体図形☆
6√2の辺が2つ。
3√2の辺が4つ。
3√2の辺が1つ。
こたえは④
28.軌跡☆
とんでもなく易しい。
こたえは⑤
ココから選択問題
問題によって難易度がまちまちなので、ひととおり目を通して、易しそうな問題だけを選ぶ。
社会科学
すべて易しい。ここでポイントを稼ぐ。
29.政治☆
日本国憲法について。
①欽定憲法ではなく民定憲法。
②軟性憲法ではなく硬性憲法。
③マッカーサー草案を受けて作成。
④法律の留保はなし。
⑤正しい。
30.政治☆
裁判所について。 本当に近年この分野がよく出るなあ。
①現在の日本に行政裁判所はない。
②知的財産高等裁判所は東京高裁の支部なので、全国8か所のすべての高等裁判所には設置されていない。
③違憲法令審査権は下級裁判所にも与えられている。
④最高裁判所裁判官の国民審査は、その人が最高裁判所裁判官に任命されて初めて行われる衆議院選挙の際に実施され、その後は最初の国民審査から10年経過して初めて行われる衆議院選挙の際に再び国民審査が行われる。つまり、参議院選挙の際には行われない。
⑤検察審査会の説明。正しい。
31.政治☆
日本の選挙制度について。小中学校レベル。
①衆議院選挙の説明。正しい。
②参議院選挙でも比例区はある。
③比例代表制は少数派政党にも議席獲得のチャンスがある。
④小選挙区は死票が多い。
⑤一票の格差について最高裁の違憲判決が出ている。
32.経済☆
国民所得について。
①国民総所得、国民純生産、国民所得の説明。正しい。
②生産、分配、支出の金額は等しい(三面等価の原則)。
③国富に対外資産は含まれる。
④ジュグラーの波ではなく、コンドラチェフの波。
⑤コンドラチェフの波ではなく、ジュグラーの波。
33.心理学☆☆
今年は資源の問題ではなくなった。
①ヤマアラシのジレンマはルソーではなくショーペンハウアー。説明も間違い。
②ホリングワースではなく、エリクソン。
③マージナルマンの説明。正しい。
④発達課題はマズローではなく、ハヴィガースト。
⑤フロイトではなくエリクソン。
人文科学
日本史でとんでもなくマニアックな奴が登場。
34.日本史☆☆☆
今年は飛鳥時代の文化。毎年文化っぽい?
①正しい。
②飛鳥寺は蘇我入鹿ではなく蘇我馬子。
③高句麗からやってきた曇徴(どんちょう)は製紙技術や絵の具、墨の作成の専門家だった。マニアック!三経義疏(さんぎょうぎしょ)は聖徳太子が著した。
④百済観音像の作者は不明。
⑤百済からやってきた観勒(かんろく)は日本に天文、暦本、陰陽道を伝えた。
35.日本史☆☆
日本の近代化について。
①幕末の日本の最大の輸出品は生糸。
②臥雲辰致は織機ではなく国産紡績機の発明者。
③座繰製糸が富岡製糸場などの機械製糸にパワーアップ。
④東海道本線は政府が敷いた最古の鉄道路線。
⑤正しい。
36.西洋史☆
宗教改革について。
①贖宥状ビジネスを行ったのはカール5世ではなくレオ10世。カール5世は教皇ではなく、ハプスブルグ家全盛期の神聖ローマ帝国の皇帝。
②ドイツ農民戦争は教皇ではなく、皇帝軍と戦った。
③カルヴァンは司教(ルターが支持)ではなく長老が協会の運営を行うべきだとした。
④エリザベス1世は英国国教会を廃止していない。
⑤正しい。
37.東洋史☆☆
不正解の選択肢の記述がめちゃマニアック。
①北宋と南宋が逆。
②形勢戸は唐代の新興貴族。中国版ユンカー的な大地主。
③正しい。
④鎮は宋代の農村の市場中心地のこと。行は商人の同業組合
⑤訓詁学が儒教の難しい用語を解説する学問。
38.地理☆
ケッペンの気候区分について。
①高山気候はケッペンの気候区分にはない。
②熱帯にステップはない。
③西岸海洋性気候の説明。
④正しい。
⑤寒帯は最も暖かい月の気温が10℃未満。
39.倫理☆
西洋哲学。
①ベーコンの説明。正しい。
②ヒュームではなくベーコンの内容。
③自我と物体の説明が逆。
④ライプニッツではなくスピノザの説明。
⑤スピノザではなくライプニッツの説明。
自然科学
物理は毎年2問とも計算みたい。
40.物理☆
仕事率。単位変換はしなくていい。
30kg × 9.8m/s² × 20m = 約6000Jの仕事を10秒で行うので
1秒あたりの仕事率は10で割って600W
答えは④
41.物理☆☆
電力損失の計算問題。ちょっとわかりにくい。
電力が1000W、電圧が200Vなので電流は5A。
W=A²×Ωなので
5²A×2Ω=50
よって電力損失は50W。
電力損失は電圧を上げると下がる(電流が下がりジュール熱が抑えられるため)。
W=V²/Ωより、電力損失は電圧の2乗に比例。
よって、電圧を5倍にすると、電力損失は1/25に抑えられる。
こたえ⑤
42.化学☆
中和滴定。価数と濃度と体積の積を合わせればよい。
濃度不明の塩酸・・・1価×χmol/L×10mL
水酸化カルシウム・・・2価×0.20mol/L×15mL
上の二つの答えを等式でつないで方程式を解く。
χ=0.60mol/L
こたえ⑤
43.化学☆
化合物や同素体について。覚えるだけの問題。易しい。
こたえは④
44.生物☆
遺伝情報とタンパク質の合成。
A:正しい。
B:DNAからRNAが転写される。
C:正しい。
D:DNA→RNA→タンパク質の順番。
こたえは②
45.生物☆
肝臓について。
①腎臓の説明。
②アルブミンを分解ではなく合成。
③正しい。
④アンモニアを尿素に変える。
⑤ホルモンの一種バソプレシンの命令で水を飲むことで塩分濃度を下げる。
46.地学☆
火山について。
A:正しい。
B:粘性が逆。
C:正しい。
D:楯状火山ではなく成層火山。
こたえは②
文学・芸術
47.漢字の読み☆
A:あんちゅうもさく
B:いちじつせんしゅう
C:うんさんむしょう
D:えいこせいすい
E:おかめはちもく
こたえは③
48.ことわざ・慣用句☆
A:どちらも肝が入る。
B:青天白日 清濁併せ呑む
C:どちらも竹が入る
D:森羅万象 神出鬼没
こたえは②
49.古典☆☆
出典は『枕草子』無名といふ琵琶
①「まろ」は一人称。「あなたのところに」ではなく「私のところに」
②正しい。
③「淑景舎の笛が欲しい僧侶の隆円は何とか答えさせようと何回もお聞きになる」
④あまりに笛が欲しい僧侶がしつこいので、中宮が代わりに「笛を交換したくないと思っています」と答えた。
⑤僧侶は笛の名前を知らなかった。
50.日本音楽☆☆☆
筝曲の有名な人物を選ぶ。
八橋はもともと琴の形をしたお菓子であるということを知っていれば判る。
でも、最近は生八橋が主流なので、苦戦は否めない。
こたえ①
- Calendar
<< March 2026 >> Sun Mon Tue Wed Thu Fri Sat 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31
- search this site.
- tags
-
- 漫画 (388)
- 脚本 (243)
- 映画 (235)
- 雑記 (165)
- ゲーム (156)
- 本 (116)
- 教育 (107)
- 生物学 (105)
- 科学 (93)
- 社会学 (81)
- 歴史 (72)
- テレビ (71)
- 芸術 (61)
- 政治 (50)
- 数学 (40)
- 進化論 (40)
- 資格試験 (38)
- 情報 (38)
- サイト・ブログ (37)
- 語学 (37)
- 映画論 (36)
- 物理学 (33)
- 哲学 (32)
- 恐竜 (29)
- 育児 (28)
- 文学 (26)
- 化学 (25)
- 論文 (22)
- PIXAR (22)
- 心理学 (18)
- 地学 (16)
- 気象学 (15)
- 地理学 (15)
- 技術 (13)
- 経済学 (12)
- 医学 (11)
- 玩具 (9)
- 司書 (8)
- 法律学 (7)
- 対談 (5)
- スポーツ (4)
- 映画の評価について (1)
- プロフィール (1)
- archives
-
- 202603 (2)
- 202602 (1)
- 202601 (2)
- 202512 (4)
- 202511 (15)
- 202510 (8)
- 202509 (5)
- 202508 (3)
- 202507 (3)
- 202506 (3)
- 202505 (1)
- 202504 (2)
- 202503 (2)
- 202502 (2)
- 202501 (1)
- 202412 (2)
- 202411 (6)
- 202410 (2)
- 202409 (4)
- 202408 (4)
- 202407 (7)
- 202406 (27)
- 202405 (11)
- 202404 (4)
- 202403 (23)
- 202402 (22)
- 202401 (15)
- 202312 (4)
- 202311 (7)
- 202310 (2)
- 202309 (8)
- 202308 (9)
- 202307 (8)
- 202306 (5)
- 202305 (15)
- 202304 (4)
- 202303 (4)
- 202302 (2)
- 202301 (4)
- 202212 (15)
- 202211 (7)
- 202210 (5)
- 202209 (4)
- 202208 (4)
- 202207 (7)
- 202206 (2)
- 202205 (5)
- 202204 (3)
- 202203 (2)
- 202202 (5)
- 202201 (6)
- 202112 (6)
- 202111 (4)
- 202110 (6)
- 202109 (7)
- 202108 (5)
- 202107 (8)
- 202106 (4)
- 202105 (8)
- 202104 (4)
- 202103 (6)
- 202102 (10)
- 202101 (3)
- 202012 (12)
- 202011 (3)
- 202010 (4)
- 202009 (5)
- 202008 (6)
- 202007 (4)
- 202006 (4)
- 202005 (4)
- 202004 (7)
- 202003 (5)
- 202002 (6)
- 202001 (8)
- 201912 (6)
- 201911 (5)
- 201910 (3)
- 201909 (4)
- 201908 (10)
- 201907 (3)
- 201906 (6)
- 201905 (10)
- 201904 (3)
- 201903 (7)
- 201902 (8)
- 201901 (5)
- 201812 (7)
- 201811 (12)
- 201810 (7)
- 201809 (5)
- 201808 (10)
- 201807 (5)
- 201806 (19)
- 201805 (14)
- 201804 (11)
- 201803 (15)
- 201802 (4)
- 201801 (6)
- 201712 (4)
- 201711 (3)
- 201710 (11)
- 201709 (9)
- 201708 (15)
- 201707 (7)
- 201706 (4)
- 201705 (5)
- 201704 (6)
- 201703 (7)
- 201702 (6)
- 201701 (3)
- 201612 (3)
- 201611 (7)
- 201610 (7)
- 201609 (2)
- 201608 (8)
- 201607 (8)
- 201606 (7)
- 201605 (3)
- 201604 (4)
- 201603 (8)
- 201602 (3)
- 201601 (2)
- 201512 (3)
- 201511 (3)
- 201510 (4)
- 201509 (4)
- 201508 (8)
- 201507 (17)
- 201506 (2)
- 201505 (5)
- 201504 (9)
- 201503 (20)
- 201502 (7)
- 201501 (4)
- 201412 (5)
- 201411 (3)
- 201410 (2)
- 201409 (3)
- 201408 (3)
- 201407 (3)
- 201406 (12)
- 201405 (6)
- 201404 (7)
- 201403 (5)
- 201402 (12)
- 201401 (9)
- 201312 (6)
- 201311 (9)
- 201310 (8)
- 201309 (6)
- 201308 (6)
- 201307 (6)
- 201306 (10)
- 201305 (10)
- 201304 (23)
- 201303 (17)
- 201302 (16)
- 201301 (5)
- 201212 (10)
- 201211 (4)
- 201210 (18)
- 201209 (4)
- 201208 (30)
- 201207 (7)
- 201206 (4)
- 201205 (6)
- 201204 (4)
- 201203 (4)
- 201202 (3)
- 201201 (3)
- 201112 (4)
- 201111 (7)
- 201110 (3)
- 201109 (9)
- 201108 (3)
- 201107 (7)
- 201106 (2)
- 201105 (11)
- 201104 (7)
- 201103 (14)
- 201102 (19)
- 201101 (27)
- 201012 (25)
- 201011 (70)
- 201010 (34)
- 201009 (30)
- 201008 (42)
- 201007 (44)
- 201006 (29)
- 201005 (37)
- 201004 (50)
- 201003 (44)
- 201002 (48)
- 201001 (38)
- 200912 (20)
- recent trackback
- others
-
- RSS2.0
- hosted by チカッパ!
- HEAVEN INSITE(本サイト)


1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | 26 | 27 | 28 | 29 | 30 | 31 | 32 | 33 | 34 | 35 | 36 | 37 | 38 | 39 | 40 | 41 | 42 | 43 | 44 | 45 | 46 | 47 | 48 | 49 | 50 | 51 | 52 | 53 | 54 | 55 | 56 | 57 | 58 | 59 | 60 | 61 | 62 | 63 | 64 | 65 | 66 | 67 | 68 | 69 | 70 | 71 | 72 | 73 | 74 | 75 | 76 | 77 | 78 | 79 | 80 | 81 | 82 | 83 | 84 | 85 | 86 | 87 | 88 | 89 | 90 | 91 | 92 | 93 | 94 | 95 | 96 | 97 | 98 | 99 | 100 | 101 | 102 | 103 | 104 | 105 | 106 | 107 | 108 | 109 | 110 | 111 | 112 | 113 | 114 | 115 | 116 | 117 | 118 | 119 | 120 | 121 | 122 | 123 | 124 | 125 | 126 | 127 | 128 | 129 | 130 | 131 | 132 | 133 | 134 | 135 | 136 | 137 | 138 | 139 | 140 | 141 | 142 | 143 | 144 | 145 | 146 | 147 | 148 | 149 | 150 | 151 | 152 | 153 | 154 | 155 | 156 | 157 | 158 | 159 | 160 | 161 | 162 | 163 | 164 | 165 | 166 | 167 | 168 | 169 | 170 | 171 | 172 | 173 | 174 | 175 | 176 | 177 | 178 | 179 | 180 | 181 | 182 | 183 | 184 | 185 | 186 | 187 | 188 | 189 | 190 | 191 | 192 | 193 | 194 | 195 | 196 | 197 | 198 | 199 | 200 | 201 | 202 | 203 | 204 | 205 | 206 | 207 | 208 | 209 | 210 | 211 | 212 | 213 | 214 | 215 | 216 | 217 | 218 | 219 | 220 | 221 | 222 | 223 | 224 | 225 | 226 | 227 | 228 | 229 | 230 | 231 | 232 | 233 | 234 | 235 | 236 | 237 | 238 | 239 | 240 | 241 | 242 | 243 | 244 | 245 | 246 | 247 | 248 | 249 | 250 | 251 | 252 | 253 | 254 | 255 | 256 | 257 | 258 | 259 | 260 | 261 | 262 | 263 | 264 | 265 | 266 | 267 | 268 | 269 | 270 | 271 | 272 | 273 | 274 | 275 | 276 | 277 | 278 | 279 | 280 | 281 | 282 | 283 | 284 | 285 | 286 | 287 | 288 | 289 | 290 | 291 | 292 | 293 | 294 | 295 | 296 | 297 | 298 | 299 | 300 | 301 | 302 | 303 | 304 | 305 | 306 | 307 | 308 | 309 | 310 | 311 | 312 | 313 | 314 | 315 | 316 | 317 | 318 | 319 | 320 | 321 | 322 | 323 | 324 | 325 | 326 | 327 | 328 | 329 | 330 | 331 | 332 | 333 | 334 | 335 | 336 | 337 | 338 | 339 | 340 | 341 | 342 | 343 | 344 | 345 | 346 | 347 | 348 | 349 | 350 | 351 | 352 | 353 | 354 | 355 | 356 | 357